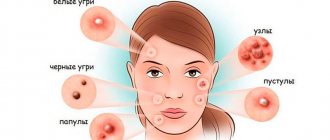
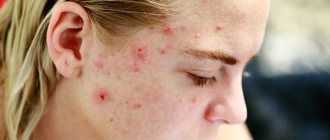
Прыщи на голове в волосах — это весьма распространенное явление. К сожалению, обычно ему не придают значения, поскольку высыпания скрыты за прядями. Как правило, пациент обращается к специалисту лишь тогда, когда проблема приобретает широкое распространение. Однако следует помнить, что лечение при этом оказывается значительно более сложным и длительным.
Почему на голове появляются прыщи?
Причины появления прыщей на голове могут быть следующими:
- нарушение деятельности сальных желез;
- неправильное питание;
- недостаточный или неправильный уход за волосами или кожей, а также неправильный выбор средств для ухода;
- гормональные нарушения или физиологические изменения (например, во время полового созревания);
- повышенное потоотделение;
- фолликулит (о его развитии могут свидетельствовать гнойные прыщи на голове);
- постоянное ношение головных уборов из синтетических материалов;
- аллергические реакции;
- частое расчесывание, травматическое воздействие;
- заболевания нервной системы;
- нарушения функционирования надпочечников;
- снижение иммунитета;
- аутоиммунные нарушения;
- наследственная предрасположенность;
- инфекционные заболевания;
- прием некоторых лекарственных препаратов (например, кортикостероидов).
Прыщи на голове у мужчин чаще всего обусловлены активностью гормонов, стрессами, воздействием химических веществ (например, во время производственной работы), а также реакцией кожи после бритья. Кроме того, высыпания могут быть результатом использования тупых лезвий триммера во время стрижки. Прыщи на голове у женщин иногда появляются при употреблении оральных контацептивов.
Также, помимо других причин, они могут сигнализировать о заболеваниях яичников, в частности, о поликистозе. Именно поэтому, если явление носит рецидивирующий характер, может потребоваться консультация гинеколога.
Как избавиться?
Чтобы окончательно устранить неприятные высыпания на коже, необходимо выяснить и исключить причины, приведшие к их появлению.
При угревой болезни очень важно придерживаться следующих принципов:
- Соблюдать правильное, здоровое питание. Как можно меньше употреблять жирной, сладкой пищи и продуктов, которые содержат большое количество простых углеводов.
- Соблюдать личную гигиену. Необходимо следить за тем, чтобы поверхность кожи лица и рук была чистой, обязательно умываться в утренние и вечерние часы. Однако стоит помнить о том, что слишком частые водные процедуры могут пересушить кожные покровы и ослабить их защитную функцию.
- Регулярно использовать кремы с антисептическим действием.
- Не выдавливать прыщи. Такие действия чреваты распространением инфекции в глубокие слои эпидермиса и усугублением воспалительного процесса.
- Не очищать кожу спиртовыми лосьонами. Данные косметические средства раздражают сальные железы и повышают их секрецию.
- Не подвергать кожные покровы активному влиянию солнечного излучения, поскольку оно повышает продукцию кожного сала.
Если акне было спровоцировано не просто неправильным питанием или несоблюдением личной гигиены, а гормональным дисбалансом или же нарушениями со стороны внутренних органов, то одного следования указанным правилам будет недостаточно для выздоровления. В таких случаях нередко специалисты назначают препараты местного или даже системного действия.
На лице
Если возникновение прыщей связано с гормональным дисбалансом, при легкой степени акне достаточно использовать местные симптоматические препараты.
Наибольшей популярностью пользуются:
- Скинорен гель.
- Дифферин гель.
- Базирон гель.
- Куриозин гель.
Обильные высыпания на коже можно подсушить с помощью простого дегтярного мыла, а также настойки календулы. С обеззараживающей, очищающей и предотвращающей воспаление целью используют местные антисептики – Ихтиоловую мазь, Метрогил гель.
В случаях, когда акне имеет 3–4 степень тяжести, назначается системная терапия, которая заключается в использовании антибактериальных (мазь Бактробан, Фузидерм крем, Зинерит в форме порошка, мазь Левомиколь) и гормональных средств (Гидрокортизоновая мазь и ее аналоги).
Применять их следует осторожно, согласно инструкции и только по назначению лечащего врача.
На теле
Прыщи у мужчин могут появляться не только на лице, но и на различных участках тела – спине, груди, руках. При легкой степени акне достаточно придерживаться здорового питания, правил личной гигиены и обрабатывать поверхность кожи средствами, которые содержат салициловую кислоту или перекись бензоила, а также косметикой на основе гликолевой или молочной кислот.
При средней и тяжелой степени акне необходима помощь специалиста. В тяжелых случаях может быть назначен Изотретиноин. Препарат обладает большим числом побочных эффектов, поэтому использовать его самостоятельно категорически запрещено. Также могут быть назначены и другие ретиноиды, антибиотики.
Лечение прыщей на голове
Курс терапии зависит от причин проблемы, однако, как правило, он включает в себя:
- антимикробные препараты;
- энтеросорбенты;
- ретиноиды;
- средства, подсушивающие высыпания.
Кроме того, эффективными в данном случае бывают такие клинические процедуры, как мезотерапия, лечение лазером, биокомплекс, плазмотерапия.
При сильном распространении высыпаний иногда требуется прием антибактериальных препаратов, а также лекарств для коррекции гормонального фона. Для профилактики повторного появления прыщей на коже головы пациенту рекомендуется правильный выбор гигиенических средств, нормализация питания, отслеживание гормонального статуса организма, соблюдение мер предосторожности при взаимодействии с химическими веществами, прием витаминов и микроэлементов, отказ от вредных привычек.
Кожные проявления патологии органов пищеварения
Кожные покровы и органы пищеварения находятся в тесной взаимосвязи, корни которой кроются в единстве происхождения в ходе эмбриогененза, общности барьерных функций, включая формирование иммунного ответа, а также взаимодействия с ассоциированной с этими органами микрофлорой. Состояние кожных покровов в значительной степени отражает состояние органов пищеварения, однако взаимосвязь патологических процессов в этих органах может иметь разноплановый характер: 1) поражение кожи может быть непосредственно обусловлено нарушением функции органов пищеварения; 2) поражение кожи может иметь общий патогенез с заболеваниями органов пищеварения, точно установленный или предполагаемый, и эти процессы идут параллельно.
Идея о том, что нарушения функции органов пищеварения естественным образом отражается на состоянии кожных покровов, хотя и витала в воздухе на протяжении тысячелетий, впервые была сформулирована в медицинской литературе William Hillary в 1759 г. [1] и развита A. Whitfield. Последний в 1932 г. ввел понятие «dermatitis colonica» [2], а один из первых подробных обзоров о влиянии на состояние кожи нарушенного кишечного всасывания был опубликован G. C. Wells только в 1962 г. [3].
Мальабсорбция макро- и микронутриентов с развитием их дефицита в организме при различных заболеваниях желудочно-кишечного тракта (ЖКТ) очевидно находит свое отражение в состоянии кожи. Чаще всего они наблюдаются при изменения кожи при нарушенном кишечном всасывании, что обусловлено мальабсорбцией цинка, меди, железа, витаминов А и PP. В ту же категорию можно отнести и развитие пурпуры как проявление гемокоагулопатии при нарушении всасывания витамина К. Селективный дефицит того или иного нутриента обычно связан с врожденным дефектом соответствующей транспортной системы кишечника, в то время как комбинированные нарушения кишечного всасывания чаще наблюдаются при генерализованном поражении кишечника (врожденного или приобретенного характера), например, при целиакии или синдроме короткой тонкой кишки. Характер поражения кожи при дефиците некоторых витаминов приведен в табл. 1 [4].
Ярким клиническим проявлением со стороны кожи является нарушение кишечного всасывание цинка. В целом причинами дефицита цинка в организме могут быть его недостаток в питании (например, при нерациональном искусственном вскармливании), различные заболевания кишечника, особенно сопровождающиеся диареей, а также врожденный дефект его кишечного всасывания (энтеропатический акродерматит).
Всасывание цинка в кишечнике тесным образом связано с характером моторики и легко развивается в случае диареи любого происхождения. Так, показано, что диарея у детей младше 1 года длительностью более 10 дней всегда сопровождается развитием дефицита цинка [5], а у детей более старшего возраста к данному состоянию может привести диарея длительностью более 14 дней [6]. При этом ускоренная кишечная моторика, нарушая всасывание цинка, способствует потере цинка, поступающего в просвет кишечника с секретами пищеварительных желез. Кроме того, дефицит цинка приводит к нарушению функции энтероцитов, что в свою очередь усугубляет его мальабсорбцию. Снижение иммунных функций на фоне дефицита цинка благоприятствует течению инфекционного процесса и также усугубляет диарею [7]. Дефицит цинка и нарушение функции энтероцитов способствуют мальабсорбции других нутриентов, в частности, натрия и воды [8]. Интересно также, что дефицит цинка приводит к снижению аппетита в результате снижения экспрессии рецепторов к нейропептиду Y в гипоталамусе и тем самым способствует уменьшению потребления пищи [9].
Энтеропатический акродерматит (синдром Брандта) характеризуется врожденным нарушением транспорта цинка через апикальную мембрану энтероцита. Заболевание передается по аутосомно-рецессивному типу и клинически проявляется характерным кожным синдромом (поражение кожи в виде везикулобуллезных высыпаний на дистальных участках конечностей и вокруг естественных отверстий), диареей и алопецией. Заболевание манифестирует после прекращения грудного вскармливания, т. к. женское молоко является важным источником цинка для ребенка в этот период жизни, с постепенным развитием основных симптомов заболевания, задержки психомоторного развития, а также снижением резистентности к инфекционным заболеваниям. Последнее обусловлено существенной ролью, которую играет цинк в функции иммунной системы, антиоксидантной защиты и даже некоторыми прямыми антиинфекционными эффектами данного микроэлемента. Похожее на энтеропатический акродерматит состояние может развиваться и вторично при тяжелой атрофии слизистой оболочки тонкой кишки, в первую очередь при целиакии. В обоих случаях для ликвидации дефицита цинка требуется назначение содержащих его препаратов.
Другой селективный дефект наблюдается при болезни Менкеса, в основе которой лежит нарушение клеточного транспорта меди в кишечнике. При этом наблюдается замедление роста, патология нервной системы, а также характерное закручивание волос, в связи с чем это заболевание получило название «болезнь закрученных или стальных волос». Болезнь связана с мутациями в гене ATP7A, кодирующем Cu(2+)-транспортирующую АТФазу, участвующую в процессах кишечного всасывания меди.
Заболевание манифестирует в неонатальном периоде, а первыми симптомами могут быть: гипотеpмия, гипеpбилиpубинемия, задержка физического развития. У части больных наблюдается образование узелков на волосах (trichorexis nodosa) и т. н. веретенообразные волосы (monilethrix). Кроме того, может наблюдаться себорейный дерматит. В течение первого полугодия жизни постепенно прогрессируют отставание в росте, задержка психомоторного развития и неврологические расстройства с утратой приобретенных в первые месяцы жизни навыков, появляются различные типы эпилептических приступов (фокальные, генерализованные, миоклонические) с формированием в дальнейшем спастического тетрапареза. Развивается трихополидистрофия: волосы спутанные, тусклые, жесткие, седые или цвета «слоновой кости».
Возможно развитие субдуральных кровоизлияний, тромботической болезни. При ангиографии в головном мозге, внутренних органах, конечностях выявляются удлиненные, извитые, варьирующего калибра артерии с чередованием областей расширения и сужения. Кроме того, могут быть выявлены дивертикулы мочевыводящей системы, предрасполагающие к инфекциям мочевого тракта. Нередко наблюдаются патологические переломы pебеp, диффузная гипопигментация кожи, а также признаки дисплазии соединительной ткани: гиперрастяжимость кожи, гиперподвижность в суставах.
Диагноз ставится на основании снижения уровня меди и церулоплазмина в сыворотке крови, низком содержании меди в биоптате печени и высоком — в слизистой оболочке кишечника и культуре клеток фибробластов кожи. В основе лечения — заместительная терапия препаратами меди.
Ниже перечислены болезни кожи, описанные в сочетании с целиакией, заболеванием с генерализованным нарушением кишечного всасывания (табл. 2) [10, 11]. Часть из них обусловлена мальабсорбцией макро- и микронутриентов, другая часть — повышенной проницаемостью кишечника на фоне атрофического процесса и повышением риска аллергического процесса, третья часть — аутоиммунным процессом в коже, который может рассматриваться как проявление основного патологического процесса. Особого обсуждения требует герпетиформный дерматит, который с целиакией имеет много общего, но также имеет и существенные отличия.
Общие механизмы поражения кожи и органов пищеварения также наблюдаются достаточно часто, например, при различных иммунопатологических процессах. При этом нарушения функции желудочно-кишечного тракта и, в частности, синдром мальабсорбции усугубляют течение кожного процесса при участии описанных выше механизмов.
При пищевой аллергии, как правило, параллельно вовлекается несколько систем организма: кожа (атопический дерматит), ЖКТ (эозинофильный эзофагит, гастрит, энтерит, колит), органы дыхания (аллергический ринит, бронхиальная астма) [12]. В последние годы пищевой аллергии придается важное значение в развитии синдрома раздраженного кишечника. Одной из точек пересечения этих заболеваний является висцеральная рецепция, которая, с одной стороны, модулируется центральными нервными влияниями, а с другой стороны — т. н. воспалением низкой активности в слизистой оболочке кишечника, главную роль в развитии которого играет дегрануляция тучных клеток. Последняя может быть обусловлена различными механизмами, в т. ч. атопическими [13].
При системных аутоиммунных заболеваниях соединительной ткани нередко наблюдается сочетанное поражение кожи и ЖКТ. Так, при системной склеродермии характерные кожные изменения сочетаются с нарушением моторики пищевода и дисфагией, нарушением моторики тонкой кишки и кишечной непроходимостью различной степени выраженности, а также синдромом нарушенного кишечного всасывания [14–18]. При системных васкулитах и ревматоидном артрите происходит параллельное поражение артерий в различных органах и системах, но впоследствии обусловленная этим процессом мальабсорбция усугубляет кожные изменения.
Воспалительные аутоиммунные заболевания кишечника, неспецифический язвенный колит и болезнь Крона также у части больных характеризуются поражением кожи. С ними нередко ассоциируются узловатая эритема и гангренозная пиодермия, имеющие единый с основным заболеванием патогенез и наблюдающиеся примерно у 3–12% больных [19–21]. Узловатая эритема проявляется безболезненными, красного цвета, подкожными узлами на разгибательных поверхностях конечностей, а ее активность соответствует активности основного заболевания [22]. При биопсии выявляется фокальный панникулит. Узловатая эритема хорошо поддается лечению глюкокортикоидными препаратами, а в резистентных случаях — инфликсимабом [23, 24]. Гангренозная пиодермия характеризуется тяжелыми изъязвлениями, отсутствием параллелизма с тяжестью заболевания и представляет серьезную проблему с точки зрения лечения терапии. При биопсии определяется стерильный абсцесс. Лечение требует применения высоких доз глюкокортикоидов, а также циклоспорина, такролимуса, мофетил микофенролата, инфликсимаба [23–26].
Развитие узловатой эритемы при болезни Крона обусловлено основным гранулематозным воспалительным процессом, а развитие тяжелой гангренозной пиодермии — неадекватной антимикробной защитой, возможно отчасти связанной со снижением продукции дефензинов в коже (как это наблюдается и в кишечнике).
Другими кожными проявлениями воспалительных заболеваний кишечника является афтозный стоматит, обычно хорошо отвечающий на течение стероидными препаратами [27, 28].
Отдельную группу составляют заболевания, при которых наблюдаются стойкие ассоциации между патологией кишечника и изменениями со стороны кожных покровов, хотя механизм данной ассоциации остается не установленным. Примером такого заболевания может быть синдром Пейтца–Йегерса.
Впервые данное заболевание было описано датским педиатром Y. Peutz в 1921 г. Под его наблюдением находилась семья, у членов которой отмечалось сочетание пигментации кожных покровов с полипозом тонкой кишки. Похожее наблюдение в 1949 г. представил H. Jeghers [29].
Синдром Пейтца–Йегерса — врожденное заболевание, передающееся по аутосомно-доминантному типу, характеризующееся пигментацией кожи и слизистых оболочек в сочетании с полипами желудочно-кишечного тракта. Пигментные пятна диаметром 1–5 мм появляются обычно в первые годы жизни, хотя описаны и у новорожденных детей, располагаясь вокруг рта, носовых отверстий, на буккальной слизистой оболочке, на кистях рук и стопах. Реже встречается перианальная и перигенитальная локализация. Интересно, что пятна, расположенные вокруг рта и носа, не исчезают со временем, тогда как выраженность пятен другой локализации может снизиться в пубертатный период. Полипы чаще всего выявляются в тощей кишке, однако встречаются и в желудке, двенадцатиперстной кишке, толстой кишке. Полипы могут стать причиной кишечной непроходимости, кровотечения, а также возможна их малигнизация. Распространенность синдрома составляет 1:120 000 живых новорожденных [30] без каких-либо половых различий [31]. Развитие его связано с мутацией гена STK11 (LKB1) с локализацией на хромосоме 19 p13.3 [32].
Ген STK11 кодирует серин-треонин киназу, модулятор клеточной пролиферации, играющей значительную роль в предотвращении развития опухолей [33]. В связи с этим фермент, кодируемый STK11, ингибирует АМФ-активируемую протеин-киназу и, опосредованно, mTOR-сигнальный путь (mammalian target of rapamycin) [34], нарушения которого выявлены у больных синдромом Пейтца–Йегерса [35].
Пигментные пятна обусловлены увеличенным числом меланоцитов в области дермоэпидермального соединения (dermoepidermal junction) с увеличением содержания меланина в базальных клетках. Полипы желудочно-кишечного тракта представляют собой гамартомы, состоящие из нормальной ткани того или иного органа, но с нарушенной его архитектоникой. Полипы при данном синдроме состоят из гландулярного эпителия и гладкомышечной ткани, соединяющейся с muscularis mucosae (мышечной пластинкой соединительной ткани).
Полипы всегда множественные. Локализуются в тонкой кишке (64%), реже в толстой кишке (53%), желудке (49%) и прямой кишке (32%). Обычно обнаруживается менее 20 полипов в каждом случае, а размер колеблется от нескольких миллиметров до 5 см в диаметре [36].
Кроме синдрома Пейтца–Йегерса гамартомные полипы наблюдаются также при ювенильном полипозе и синдроме гамартомных опухолей, ассоциированных с геном PTEN (PTEN hamartoma tumor syndrome). К последним относятся синдром Cowden, синдром Bannayan–Riley–Ruvalcaba и другие, обусловленные мутацией данного гена.
Дифференциальный диагноз пигментных поражений проводится с синдромами LEOPARD, Langier–Hunziker, Carney, Cowden и нормальным состоянием кожи, наблюдающимся у части афроамериканцев [37, 38].
Особый интерес представляет анализ взаимосвязи герпетиформного дерматита Дюринга и целиакии. С одной стороны, в патогенезе обоих заболеваний лежит непереносимость злакового белка глютена с развитием атрофии слизистой оболочки тонкой кишки и, как следствие, генерализованного нарушения кишечного всасывания. Последнее в наибольшей степени выражено при целиакии, хотя существует значительное число атипичных форм, при которых кишечный синдром уходит на второй план. Часто атипичная целиакия проявляется железодефицитной анемией, или остеопорозом, или низкорослостью, а также многими другими внекишечными симптомами. Герпетиформный дерматит Дюринга не является атипичной формой целиакией, но самостоятельным заболеванием, при котором у глютен-чувствительных лиц развивается характерное поражение кожи.
Как при целиакии, так и при герпетиформном дерматите можно выявить характерный HLA-гаплотип, циркулирующие антитела к тканевой трансглутаминазе, а также атрофию ворсинок слизистой оболочки тонкой кишки с положительным эффектом на ее состояние безглютеновой диеты. Следует, однако, отметить, что примерно у 20% больных с герпетиформным дерматитом состояние слизистой оболочки тонкой кишки остается нормальным [39, 40].
Клинически герпетиформный дерматит проявляется герпетиформно сгруппированными полиморфными элементами (пузырьки, пузыри, пустулы, папулы и папуло-везикулы) на неизмененных или отечных эритематозных участках кожи, появляющимися одновременно или с небольшими интервалами. Покрышка пузыря плотная. Содержимое пузыря первоначально прозрачное, затем — мутное. Пузыри могут превращаться в пустулы, вскрываться с образованием эрозий, на поверхности которых образуются корки с последующей эпителизацией. По периферии таких участков могут возникать волдыри. Сыпь обычно располагается симметрично и группируется в виде колец, полуколец или гирлянд (герпетиформная группировка). Типичными местами локализации являются разгибательные поверхности конечностей и ягодицы. Появлению сыпи нередко предшествует или сопутствует общее недомогание, головные боли, бессонница, диспептические явления, повышение температуры от 37,5 до 40 °C. Зуд обычно резко выражен, иногда возможно чувство жжения. Обострение болезни продолжается в течение нескольких недель, причем на одних участках сыпь разрешается, проходя стадию вторичных элементов (эрозии, чешуйки, корочки, гипер- или гипопигментация), а на других появляются свежие высыпания. На волосистой части головы высыпания отсутствуют. У детей довольно часто поражаются слизистые оболочки [41], наблюдается повышенная склонность к образованию пустул.
Патогенез обоих заболеваний остается до конца нераскрытым. В то же время характер патологического процесса в коже отличается от такового в тонкой кишке и характеризуется присутствием воспалительного инфильтрата, преимущественно состоящего из нейтрофилов, локализованного в дермальных сосочках, где обнаруживают и депозиты IgA [42]. Значение нейтрофилов в патологическом процессе подтверждается положительным эффектом на кожные изменения назначения дапсона, подавляющего активность нейтрофилов. На это же указывает повышенная экспрессия CD11b, некоторое снижение L-селектина и повышение функции рецепторов FcIgA [43]. В то же время в тонкой кишке как при целиакии, так и при герпетиформном дерматите наблюдается преимущественно мононуклеарная реакция.
Обращает на себя внимание также то, что безглютеновая диета, эффективная при целиакии, недостаточно действенна при герпетиформном дерматите, требующем дополнительного назначения специфических препаратов.
Таким образом, взаимосвязь кожного и кишечного процесса при герпетиформном дерматите остается неясной, хотя очевиден параллелизм указанных нарушений.
Особое внимание в последние десятилетия к себе привлекает инфекция Helicobacter pylori (H. pylori), первоначально ассоциированная с развитием хронического гастрита и язвенной болезни. В дальнейшем было установлена возможная роль данного инфекционного агента в развитии значительного числа заболеваний, включая кожные (табл. 3) [44].
Значительное число исследований посвящено изучению связи инфекции H. pylori и хронической крапивницы, под которой подразумевают хроническое кожное заболевание, характеризующиеся периодически возникающими зудящими волдырями без явной связи с физическими и алиментарными факторами. Характер этой взаимосвязи до конца не установлен. Одна из гипотез предполагает повышение кишечной проницаемости на фоне хеликобактерной инфекции для различных агентов, способных вызывать дегрануляцию тучных клеток [45]. Другие гипотезы приписывают H. pylori иммуномодулирующее действие. В частности, в сыворотке крови больных с хронической крапивницей были выявлены антитела IgG и IgA к ассоциированному с H. pylori 19-kDa-липопротеину [46, 47]. Также обнаруживаются аутоантитела класса IgG к IgE и Fc-εRiα и предполагается возможность продукции при хеликобактерной инфекции антител в связи с молекулярной мимикрией [48]. Исследования, направленные на оценку эффективности эрадикации H. pylori при хронической крапивнице, носят противоречивый характер. Однако тщательно спланированное исследование E. Magen и соавт. показало достоверное снижение активности процесса у пациентов, которым лечение проводилось, по сравнению с теми, кто лечение не получал [49].
В этой связи обсуждается значение H. pylori в развитии атопического дерматита. Так, G. Corrado и соавт. показали положительную ассоциацию пищевой аллергии с хеликобактерной инфекцией в группе, в которую вошли 30 детей с различными гастроинтестинальными жалобами [50]. В исследовании I. H. Galadari и соавт. частота выявления H. pylori у больных с атопическим дерматитом была достоверно выше, по сравнению с контролем [51]. K. Murakami и соавт. описали случай успешного лечения атопического дерматита у 14-летней девочки, которой была проведена эрадикация H. pylori [52]. Тем не менее, многие аспекты рассматриваемой взаимосвязи остаются противоречивыми.
Предполагается также, что хеликобактерная инфекция может быть пусковым фактором развития псориаза [54–56], однако механизмы его развития неизвестны.
Таким образом, болезни органов пищеварения оказывают значительное влияние на состояние кожи, а симптомы ее поражения могут свидетельствовать о поражении ЖКТ. Механизмы этой взаимосвязи могут быть различны, а в ряде случаев остаются до конца непознанными. Тем не менее, при развитии кожного патологического процесса следует исключить заболевания пищеварительной системы, а при гастроэнтерологической патологии следует внимательно следить за состоянием кожи, что может иметь значение для оценки активности процесса, его прогноза и назначения адекватной терапии как в гастроэнтерологической, так и в дерматологической практике.
Литература
- Hiliary W. Observations on the Changes of the Air and the Concomitant Epidemical Diseases in the Island of Barbados. London: Hitch and Harris, 1759.
- Whitfield A. On a hitherto undescribed disease of the skin // Brit. J. Derm. 1932; 44: 24–28.
- Wells G. C. Skin disorders in relation to malabsorption // Brit. med. J. 1962; 2: 937–943.
- Thrash B., Patel M., Shah K. R., Boland C. R., Menter A. Cutaneous manifestations of gastrointestinal disease. Part II // J Am Acad Dermatol. 2013; 68: 211.e1–33.
- Naveh Y., Lightman A., Zinder, O. Effect of diarrhea on serum zinc concentrations in infants and children // J. Pediatr. 1982; 101: 730–732.
- Black R. E., Sazawal S. Zinc deficiency and zinc supplementation for childhood diarrhea in developing countries // J. Am. Coll. Nutr. 1998; 17: 516.
- Wapnir R. A. Zinc Deficiency, Malnutrition and the Gastrointestinal Tract // J. Nutr. 2000; 130: 1388S-1392S.
- Ghishan F. K. Transport of electrolytes, water and glucose in zinc deficiency // J. Pediatr. Gastroenterol. Nutr. 1984; 3: 608–612.
- Lee R. G., Rains T. M., Tovar-Palacio C., Beverly J. L., Shay N. F. Zinc deficiency increases hypothalamic neuropeptide Y and neuropeptide Y mRNA levels and does not block neuropeptide Y-induced feeding in rats // J. Nutr. 1998; 128: 1218–1223.
- Humbert P., Pelletier F., Dreno B., Puzenat E., Aubin F. Gluten intolerance and skin diseases // Eur J Dermatol. 2006; 16: 4–11.
- Abenavoli L., Proietti I., Leggio L., Ferrulli A., Vonghia L., Capizzi R., Rotoli M., Amerio P. L., Gasbarrini G., Addolorato G. Cutaneous manifestations in celiac disease // World J Gastroenterol. 2006; 12: 843–852.
- Lied G. A. Gastrointestinal food hypersensitivity: Symptoms, diagnosis and provocation tests // Turk J Gastroenterol. 2007; 18 (1): 5–13.
- Zar S., Kumar D., Benson M. J. Review article: food hypersensitivity and irritable bowel syndrome // Aliment Pharmacol Ther. 2001; 15: 439–449.
- Psachey R. D. G., Creamer B., Pierce J. W. Sclerodermatous involvement of the stomach and the small and large bowel // Gut. 1969; 10: 285–292.
- Marks J., Shuster S. Intestinal malabsorption and the skin // Gut. 1971, 12: 938–947.
- Carron D. B., Douglas A. P. Steatorrhoea in vascular insufficiency of the small intestine // Quart. J. Med. 1965; 34331–34340.
- Booth C. C. The enterocyte in coeliac disease // Brit. Med. J. 1970; 4: 1–17.
- Marks J., Shuster S. Intestinal malabsorption and the skin // Gut. 1971; 12: 938–947.
- Veloso F. T., Carvalho J., Magro F. Immune-related systemic manifestations of inflammatory bowel disease: A prospective study of 792 patients // J Clin Gastroenterol. 1996; 23: 29–34.
- Bernstein C. N., Blanchard J. F., Rawsthorne P., Yu N. The prevalence of extraintestinal diseases in inflammatory bowel disease: a population-based study // Am J Gastroenterol. 2001; 96: 1116–1122.
- Rankin G. B., Watts H. D., Melnyk C. S., Kelley M. L., Jr. National Cooperative Crohn’s disease study: extraintestinal manifestations and perianal complications // Gastroenterology. 1979; 77: 914–920.
- Rothfuss K. S., Stange E. F., Herrlinger K. R. Extraintestinal manifestations and complications in inflammatory bowel diseases // World J Gastroenterol. 2006; 12: 4819–4831.
- Veloso F. T. Review article: skin complications associated with inflammatory bowel disease // Aliment Pharmacol Ther. 2004; 20 (Suppl 4): 50–53.
- Clayton T. H., Walker B. P., Stables G. I. Treatment of chronic erythema nodosum with infliximab // Clin Exp Dermatol. 2006; 31: 818–825.
- Loftus E. V. Management of extraintestinal manifestations and other complications of inflammatory bowel disease // Curr Gastroenterol Rep. 2004; 6: 506–513.
- Regueiro M., Valentine J., Plevy S., Fleisher M. R., Lichtenstein G. R. Infliximab for treatment of pyoderma gangrenosum associated with inflammatory bowel disease // Am J Gastroenterol. 2003; 98: 1821–1826.
- Mintz R., Feller E. R., Bahr R. L., Shah S. A. Ocular manifestations of inflammatory bowel disease // Inflamm Bowel Dis. 2004; 10: 135–139.
- Evans P. E., Pardi D. S. Extraintestinal manifestations of inflammatory bowel disease: focus on the musculoskeletal, dermatologic, and ocular manifestations // MedGenMed. 2007. 19; 9 (1): 55–56.
- Jeghers H., McKusick V. A., Katz K. H. Generalized intestinal polyposis and melanin spots of the oral mucosa, lips and digits; a syndrome of diagnostic significance // N Engl J Med. 1949; 241 (25): 993.
- Lindor N. M., Greene M. H. The concise handbook of family cancer syndromes. Mayo Familial Cancer Program // J Natl Cancer Inst. 1998; 90 (14): 1039–171.
- Bishop P., Loftis S., Nowicki M. What syndrome is this? Peutz–Jeghers syndrome // Pediatr Dermatol. 2004; 21 (4): 503–505.
- Hemminki A., Markie D., Tomlinson I., avizienyte E., Roth S., Loukola A., Bignell G., Warren W., Aminoff M., Höglund P., Järvinen H., Kristo P., elin K., Ridanpää M., Salovaara R., Toro T., Bodmer W., Olschwang S., Olsen A. S., Stratton M. R., De La Chapelle A., Aaltonen L. A. A serine/threonine kinase gene defective in Peutz–Jeghers syndrome // Nature. 1998; 391 (6663): 184–187.
- Spigelman A. D., Thomson J. P., Phillips R. K. Towards decreasing the relaparatomy rate in the Peutz–Jeghers syndrome: the role of preoperative small bowel endoscopy // Br J Surg. 1990; 77 (3): 301–302.
- Lin B. C., Lien J. M., Chen R. J., Fang J. F., Wong Y. C. Combined endoscopic and surgical treatment for the polyposis of Peutz–Jeghers syndrome // Surg Endosc. 2000; 14 (12): 1185–1187.
- Zbuk K. M., Eng C. Hamartomatous polyposis syndromes // Nat Clin Pract Gastronenterol Hepatol. 2007; 4 (9): 492–502.
- Giardiello F. M., Trimbath J. D. Peutz–Jeghers syndrome and management recommendations // Clin Gastroenterol Hepatol. 2006; 4 (4): 408–415.
- Erbe R. W. Inherited gastroinestinal-polyposis syndromes // N Engl J Med. 1976; 294 (20): 1101–1104.
- Utsunomya J., Gocho H., Miyanaga T., Hamaguchi E., Kashimure A. Peutz–Jeghers syndrome: its natural course and management // Johns Hopkins Med J. 1975; 136 (2): 71–82.
- Kaukinen K., Collin P., Maki M. Latent coeliac disease or coeliac disease beyond villous atrophy? // Gut. 2007; 56 (10): 1339–1340.
- Troncone R., Jabri B. Coeliac disease and gluten sensitivity // Journal of Internal Medicine. 2011; 269 (6): 582–590.
- Скрипкин Ю. К., Шарапова Г. Я. Кожные и венерические болезни. М.: Медицина, 1987, 168–177.
- Warren S. J. P., Cockerell C. J. Characterization of a subgroup of patients with dermatitis herpetiformis with nonclassical histologic features // American Journal of Dermatopathology. 2002; 24 (4): 305–308.
- Smith A. D., Streilein R. D., Hall III R. P. Neutrophil CD11b, L-selectin and Fc IgA receptors in patients with dermatitis herpetiformis // British Journal of Dermatology. 2002; 147 (6): 1109–1117.
- Hernando-Harder A. C., Booken N., Goerdt S., Singer M. V., Harder H. Helicobacter pylori infection and dermatologic diseases // J Dermatol. 2009; 19 (5): 431–444.
- Buhner S., Reese I., Kuehl F., Lochs H., Zuberbier T. Pseudoallergic reactions in chronic urticaria are associated with altered gastroduodenal permeability // Allergy. 2004; 59: 1118–1123.
- Bakos N., Fekete B., Prohaszka Z., Fust G., Kalabay L. High prevalence of IgG and IgA antibodies to 19-Da Helicobacter pylori-associated lipoprotein in chronic urticaria // Allergy. 2003; 58: 663–667.
- Mini R., Figura N., D’Ambrosio C. et al. Helicobacter pylori immunoproteomes in case reports of rosacea and chronic urticaria // Proteomics. 2005; 5: 777–787.
- Appelmelk B. J., Simoons-Smit I., Negrini R. et al. Potential role of molecular mimicry between Helicobacter pylori lipopolysaccharide and host Lewis blood group antigens in autoimmunity // Infect Immun. 1996; 64: 2031–2040.
- Magen E., Mishal J., Schlesinger M., Scharf S. Eradication of Helicobacter pylori infection equally improves chronic urticaria with positive and negative autologous serum skin test // Helicobacter. 2007; 12: 567–571.
- Corrado G., Luzzi I., Lucarelli S. et al. Positive association between Helicobacter pylori infection and food allergy in children // Scand J Gastroenterol. 1998; 33: 1135–1139.
- Galadari I. H., Sheriff M. O. The role of Helicobacter pylori in urticaria and atopic dermatitis // Skinmed. 2006; 5: 172–176.
- Murakami K., Fujioka T., Nishizono A. et al. Atopic dermatitis successfully treated by eradication of Helicobacter pylori // J Gastroenterol. 1996; 31 (Suppl 9): 77–82.
- Valencak J., Trautinger F., Fiebiger W. C., Raderer M. Complete remission of chronic plaque psoriasis and gastric marginal zone B-cell lymphoma of MALT type after treatment with 2-chlorodeoxyadenosine // Ann Hematol. 2002; 81: 662–665.
- Saez-Rodriguez M., Noda-Cabrera A., Garcia-Bustinduy M. et al. Palmoplantar pustulosis associated with gastric Helicobacter pylori infection // Clin Exp Dermatol. 2002; 27: 720.
- Raderer M., Osterreicher C., Machold K. et al. Impaired response of gastric MALT-lymphoma to Helicobacter pylori eradication in patients with autoimmune disease // Ann Oncol. 2001; 12: 937–939.
Н. Г. Короткий, доктор медицинских наук, профессор Н. М. Наринская С. В. Бельмер1, доктор медицинских наук, профессор
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
1 Контактная информация
Abstract. Alimentary organ diseases have strong impact on skin condition and the symptoms of its affection may indicate affection of alimentary organ. The article covers relations between bowel pathology and changes of cutaneous covering in cases of Brandt’s syndrome, Peutz–Jeghers’ syndrome, Crohn’s disease, interconnection of dermatitis herpetiformis and celiac disease. Authors also analyze the role of H. pylori in development of atopic dermatitis.
О причинах гормонального дисбаланса
У молодых мужчин причины гормонального расстройства связаны со следующими факторами:
- Нарушена работа щитовидной железы, гипофиза, яичек или других желез, ответственных за выработку гормонов. Сбои могут быть обусловлены врожденными патологиями либо приобретенными аномалиями.
- Половые железы перестали нормально вырабатывать гормоны из-за ушибов, опухолевых процессов, воздействия инфекционных возбудителей.
- Токсическое воздействие агрессивных жидкостей, бытовой химии и косметики.
- Асоциальный образ жизни, наличие алкогольной или наркотической зависимости, злостное табакокурение.
У возрастных мужчин главные причины андрогенной недостаточности кроются в том, что снижается функция половых желез, как следствие этого – меньше вырабатывается тестостерона. При этом увеличивается количество эстрогенов (женских гормонов), развивается ожирение. Образуется порочный круг, когда уменьшение андрогенов приводит к ожирению, что усиливает синтез лептина (гормона жировой ткани), еще больше угнетающий синтез тестостерона.
Обратите внимание! Употребление большого количества пива часто приводит к гормональным сбоям.
Вне зависимости от возраста, нарушение выработки гормонов может быть связано со следующими факторами:
- слабая физическая активность;
- сердечно-сосудистые заболевания;
- патологии почек;
- повышенный уровень холестерина и глюкозы;
- нерациональное питание;
- ожирение;
- частые стрессы, бессонница, хроническое утомление;
- перегрев яичек (в том числе – при крипторхизме).