Что мы знаем о родинках?
Что мы всегда слышали о родинках: «Не мешает? Живите спокойно, не трогайте вы свою родинку!». Этот весьма расхожий в прошлом совет убеждал нас в том, что изначально данные природой или появляющиеся с годами родинки должны оставаться неприкосновенными. А тронешь — не избежать беды. Отчасти это, правда – действительно, самостоятельное удаление родинок может привести к самым печальным последствиям. Но справедливости ради следует также отметить, что далеко не каждая родинка нуждается в удалении. Самые безобидные — плоские родинки
(от розового до темно-коричневого цвета). Обычно они ведут себя «смирно», не травмируются и не создают неудобств. Единственное, о чем нужно помнить — о защите таких родинок (на открытых участках тела) от солнечных лучей. К
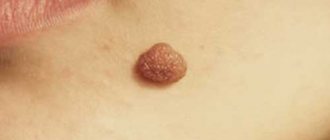
выпуклым родинкам
, тем более, если они часто задеваются одеждой, нужно относиться более внимательно. Если они есть на спине и на других недоступных вашему взгляду местах, наблюдение за ними нужно поручить кому-нибудь из близких. И, разумеется, если произойдут какие-то изменения — родинка станет больше, из плоской превратиться в выпуклую или изменит свои очертания, надо сразу же обратиться к специалисту.
В каком случае воздействие йода может навредить
Опасность применения препарата скрыта в последствиях. Имеются причины, по которым не следует пользоваться таким видом прижигания:
- Раствор оказывает стимулирующее действие на кровообращение, провоцирующее быстрый рост невуса. Запускает процесс перерождения клеток в злокачественную опухоль.
- Имеется риск ожога, может вызывать серьезные осложнения.
- Возможно занесение инфекции, начало воспалительного процесса.
- Из-за окрашивающих свойств средства (коричневый цвет напоминает естественный цвет родимых пятен), появляются трудности с наблюдением за доброкачественным невусом. Можно пропустить процесс преобразования в злокачественную опухоль.
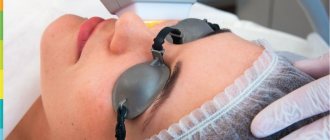
Современная медицина предусмотрела безопасные способы удаления нежелательных образований на теле, без вреда для здоровья. Убирать невусы, бородавки, папилломы можно с помощью лазерного, радиоволнового метода, криотерапии, хирургического вмешательства. Иссечение происходит безболезненно, не остаются следы и шрамы. Не требуется повторное удаление, за исключением редких случаев.
При малейших изменениях родинки: появился зуд, жжение, изменился цвет или форма, размер, не стоит ковырять и лечить самостоятельно невус, особенно прижигать.
Перед визитом к врачу, нежелательно мазать родинку йодом – это влияет на естественный цвет образования и затрудняет диагностику.
Не забывайте также о противопоказаниях удаления родинок йодом. К ним относят:
- аллергическая реакция на жидкость или ее компоненты;
- в период беременности, кормления грудью ребенка;
- дети младше трех лет;
- болезни щитовидной железы, почек, печени хронического течения;
- повышенная чувствительность к средству;
- туберкулез легких;
- если образования расположены в опасных зонах (лица, веки, слизистая оболочка, интимные зоны).
Никакой самостоятельности.
Некоторые считают, что родинки можно удалять самому, перевязывая их, например, шелковой нитью. Это глубокое заблуждение. Попытки перевязывать бородавки, папилломы тонкой шелковой нитью зачастую только провоцирует рост этих образований. Сегодня в продаже есть препараты на основе чистотела, предназначенные для сведения бородавок. Но ни родинки, ни папилломы, ни бородавки лучше не удалять самостоятельно никакими средствами. Сок чистотела по своему составу схож с йодом, поэтому длительное воздействие препарата вызывает ожог кожи. Прижигание йодом еще более опасно — он агрессивнее чистотела. Усердно стараясь избавиться от папиллом при помощи йода, вы можете получить рубцы на коже. Грамотно удалить родинку может только дерматолог.
Преимущества и недостатки удаления родинки йодом
Йод – распространенный препарат, обладающий бактерицидным, противогрибковым эффектом, дезинфицирует кожу. Благодаря своему составу, средство уменьшает выработку меланина, убирая пигментацию кожи. Прижигать родинки йодом можно только после обследования и выявления доброкачественной природы образования. Способ обладает рядом преимуществ:
- доступная цена;
- доступность препарата (можно приобрести в любом аптечном пункте);
- практически не имеет противопоказаний;
- эффективность;
- лечение можно проводить в домашних условиях;
- побочные эффекты минимальные.
Как и все медицинские препараты, препарат имеет недостатки в применении, к ним относят:
- не рекомендуется выжигать невусы больших размеров, новообразование останется на месте;
- возможен ожог кожного покрова;
- аллергическая реакция на некоторые компоненты средства.
Регулярное прижигание йодом оказывает деструктивное воздействие на образование, уменьшая его в размере и подсушивая.
Невус покрывается корочкой, сдирать которую не рекомендуется. Она должна отпасть самостоятельно. Лечению поддаются единичные папилломы, висячие и красные бородавки. Это один из бюджетных, эффективных народных методов удаления наростов в домашних условиях. Действие направлено на уничтожение клеток, пораженных вирусом.
Методы удаления.
Удаление родинок и бородавок
- Стоимость: 2 000 руб.
Подробнее
Удаление родинок может проводиться с помощью лазера, радиоволновой коагуляции либо электрической коагуляции. Эти манипуляции проводятся в амбулаторных условиях под местным обезболиванием. Выбор метода лечения определяется врачом в каждом конкретном случае. На мой взгляд, наиболее эффективным и безболезненным является метод радиоволновой коагуляции. Данная методика применяется нами в большинстве случаев, хотя в некоторых случаях мы используем иссечение обычными хирургическими инструментами с дальнейшим наложением швов. При использовании радиоволновой коагуляции повреждение ткани при заборе материала будет минимальными, уменьшаются кровопотери, сокращается реабилитационный период, в то время как, например, при лазерном методе процесс заживления растягивается на достаточно длительный срок. Повторные образования после удаления не появляются, но при несоблюдении мер предосторожности самим пациентом может возникнуть инфицирование.
Как свести родинку йодом
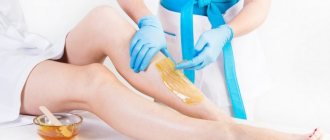
Зная правила использования средства, можно избежать неприятных последствий, осложнений. Чтобы процедура прошла эффективно и безопасно, прижигать образование нужно следующим способом:
- йод не разбавлять, поскольку сводить невусы быстрее средство не будет;
- для увеличения скорости проникновения в эпителий, рекомендуется перед процедурой распарить тело, приняв горячий душ или ванну;
- перед процедурой следует нанести на кожу вокруг нароста жирный крем или вазелин. Это поможет избежать повреждения здоровых участков кожи;
- не прикладывайте на образование ватный диск или марлю, смоченную в растворе, на длительное время. Это чревато воспалением пораженного места, появлением зуда, жжения, красноты;
- во избежание шрамов и рубцов не рекомендуется сковыривать, отрывать образовавшуюся корочку. Она должна отслоиться самостоятельно;
Инструкция по выведению образований с помощью йода:
- перед тем как родинку мазать йодом, обработайте кожу антисептическим средством или мылом;
- аккуратно подсушить обработанное место полотенцем;
- для защиты кожи смазать кремом или вазелином вокруг нароста;
- смочить ватную палочку в растворе;
- наносить точечно на образование, избегая попадания на здоровые участки эпителия.
Обработка делается дважды в сутки, на протяжении двух недель. За это время бородавки и родинки засыхают и отпадают. Продолжать мазать участок до полного засыхания нароста. Прижечь родинку йодом, если сковырнул или оторвал нельзя, лучше обработать антисептическим средством, проконсультироваться с дерматологом о возможном ее удалении. Обработка поврежденного невуса должна быть только по разрешению врача.
Не рекомендуется пользоваться методом людям с низким болевым порогом и чувствительной кожей. Возможно появление зуда, жжения, покраснения.
Для борьбы с папилломавирусом эффективным средством является синий йод (в аптеке продается под названием «Йодинол»). Препарат принимается внутрь, назначается только врачом. Эффективно уничтожает зараженные клетки вирусом, блокируя их дальнейшее распространение по организму, улучшает работу желудочно-кишечного тракта.
Оставленные без внимания родинки.
Некоторые из видов родинок способны перерождаться в одну из самых злокачественных опухолей — меланому (рак кожи). Исходным местом образования большинства меланом являются врожденные пигментные пятна и бородавчатые родинки. Как начинается это опасное развитие?
Например, после повреждения человек лишь замечает, как цвет родинки начинает меняться, она увеличивается, трескается, превращается в язвочку, подчас и в опухоль. Поэтому, не впадая в панику, обращайте внимание на вышеуказанные симптомы, особенно на прогрессирующее увеличение родинки, изменение ее цвета. Если все эти симптомы имеют место быть, немедленно поспешите к дерматологу. Неблагоприятный прогноз меланомы диктует необходимость регулярного наблюдения у врача. Помимо факторов-раздражителей (ультрафиолетовое облучение, травма), причиной развития меланомы могут быть также генетические и эндокринные факторы. Однако на первом же месте стоит, безусловно, чрезмерное пребывание на солнце. Ультрафиолетовое облучение в больших дозах вызывает необратимые изменения в клетках кожи, многократно увеличивая риск их перерождения. Наиболее подвержены мутагенному воздействию солнечных лучей светлокожие и светловолосые, рыжеволосые люди с голубыми и серыми глазами. К группе риска относятся также и те, у кого много веснушек, пигментных пятен и родинок.
Влияние повидон-йода на эрадикацию высокоонкогенных типов ВПЧ у женщин с поражением шейки матки
Актуальность
За последнее десятилетие достигнуты значительные успехи в понимании роли вируса папилломы человека (ВПЧ) в развитии рака шейки матки (РШМ) и других аногенитальных раков. ВПЧ является основным этиологическим агентом дисплазии шейки матки и карциномы [1]. РШМ — третий по распространенности гинекологический рак в развитых странах. В России число смертей от РШМ увеличилось на 3500 женщин в год. Приблизительно половину пациенток с РШМ составляют женщины репродуктивного возраста (моложе 50 лет) [2]. В последнее время по этой причине ежегодно умирают более 200 женщин в возрасте 20–39 лет. ВПЧ является распространенным вирусом, который передается горизонтально через гетеросексуальный контакт. Примерно 80% всех женщин инфицированы ВПЧ в какой-то момент их жизни, но при этом у порядка 90% папилломавирусная инфекция (ПВИ) спонтанно регрессирует в течение нескольких лет. При отсутствии самостоятельной элиминации может развиваться РШМ. Практически 100% плоскоклеточных интраэпителиальных поражений и РШМ, порядка 43% опухолей вульвы и 70% опухолей влагалища связаны с ПВИ, ежегодно вызывающей 530 тыс. новых случаев РШМ и 21 тыс. случаев рака вульвы и влагалища во всем мире [3]. При отсутствии скрининговой стратегии наблюдается рост заболеваемости РШМ и раком вульвы у молодых женщин [4]. ВПЧ представляет собой двуцепочечный ДНК-вирус, принадлежащий к роду Papilloma
в семействе
Papovaviridae
[5]. Установлено, что ВПЧ — наиболее частая сексуально-трансмиссионная инфекция, являющаяся основной причиной цервикальных плоскоклеточных интраэпителиальных поражений и инвазивного РШМ. Выделяют более 100 типов, инфицирующих эпителий полового тракта. Передача ВПЧ происходит в первую очередь путем контакта кожи с кожей и, вероятно, при нарушении целостности эпидермиса, при этом вирус может инфицировать базальные клетки плоского эпителия [6].
Типы ВПЧ и их роль в развитии онкологических процессов
На сегодняшний день в женском репродуктивном тракте идентифицировано более 100 генотипов ВПЧ. 13 типов ВПЧ (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 и 68) признаны высокоонкогенными (13HR), вызывающими рак. Тем не менее другие типы ВПЧ также могут быть связаны с развитием рака. По данным N. Munoz, два дополнительных типа ВПЧ — 73 и 82 — следует считать канцерогенными. G. Halec et al. на основании систематического обзора продемонстрировали, что 26, 53, 66, 67, 68, 70, 73 и 82 типы ВПЧ могут быть онкогенными [7]. Одна из наиболее важных проблем заключается в том, что диагностика на основе полимеразной цепной реакции (ПЦР), используемая в эпидемиологических исследованиях, имеет ограничения. Во-первых, метод ПЦР обнаруживает не только высокоонкогенные, но и другие типы ВПЧ. Во-вторых, некоторые ПЦР-тесты с использованием консенсусных праймеров показали несогласованные результаты в определении типов ВПЧ, т. к. чувствительность детекции у некоторых типов ВПЧ ниже, чем у других. Типы ВПЧ с низким риском, такие как 6, 11, 40, 42, 43, 44 и 54, связаны с генитальными бородавками и аногенитальными поражениями низкого уровня риска [8]. ВПЧ 16 и 18 типов с высоким риском вместе составляют порядка 70% случаев РШМ, в то время как ВПЧ 6 и 11 типов с низким риском ответственны за 90% генитальных бородавок [9]. Иммунная система играет важную роль в контроле развития рака. Геном ВПЧ кодирует два онкопротеина — Е6 и Е7, способные инактивировать белки р53, и ретинобластомы (pRB) — регуляторы пролиферативной активности клеток. Они необходимы для возникновения и поддержания злокачественного клеточного фенотипа [10]. Адаптивный иммунный ответ защищает от ВПЧ-индуцированных заболеваний [11]. Прогрессирование заболеваний, вызванных ВПЧ, связано с отсутствием сильного ВПЧ-специфического ответа CD4+ и CD8+ Т-клеток. Химиотерапия или лучевая терапия влияет на иммунную регуляторную активность и в сочетании с вакцинацией потенцирует эффективный локальный ВПЧ-специфический Т-клеточный иммунитет в опухолевых моделях мышей. Успешное лечение ВПЧ-индуцированных поражений может быть достигнуто с помощью низкодозированного циклофосфамида, изменяющего местный иммунитет. С учетом важности локального микроокружения в персистенции ВПЧ-индуцированных поражений и опухолей эффективными могут быть методы лечения, способные на местном уровне сместить баланс иммуноэффекторов, таких как ингибиторы циклооксигеназы-2, за счет продукции простагландина Е2 и трансформирующего фактора роста β [12]. В карциноме вульвы выделяют два отдельных канцерогенных пути, один из которых связан с ВПЧ 16 типа. Это четвертый по распространенности инвазивный гинекологический рак, который поражает в основном пожилых женщин и чаще встречается в западных странах [13]. Прогностические факторы течения заболевания включают наличие или отсутствие метастазов в лимфатических узлах, а также размер опухоли и ее рецидивы. Рецидив (гематогенные метастазы) отмечается у 40% пациенток. Прогностическая роль ВПЧ при раке вульвы обсуждается, некоторые исследования показали лучшую выживаемость женщин с ВПЧ-положительными опухолями вульвы, другие — нет [14]. Важным вопросом остается организация скрининговых программ. Такие программы эффективно проводятся в Новой Зеландии. В национальных рекомендациях по программе скрининга РШМ принято всем женщинам в возрасте от 20 до 69 лет, которые когда-либо имели половой акт, назначать цитологический мазок шейки матки в течение 3 лет. Если это первичный скрининговый мазок или с момента предыдущего исследования прошло более 5 лет, рекомендуется второй мазок повторить через год после первого, а затем через 3 года. После введения данной скрининговой программы значительно снизилась заболеваемость РШМ, составляющая в настоящее время 5,4 на 100 тыс. женщин [15]. Помимо этого, в Новой Зеландии было выполнено масштабное исследование по распределению генотипов ВПЧ в образцах шейки матки. Материал был собран у женщин, имеющих высокоонкогенные типы ВПЧ (в 2009–2011 гг.) или страдающих инвазивным РШМ (в 2004–2010 гг.). Наиболее распространенными типами ВПЧ, вызывающими неоплазии шейки матки (цервикальная интраэпителиальная неоплазия — CIN 2 и 3), были типы ВПЧ 16 (51%), 52 (19%), 31 (17%), 33 (13%) и 18 (12%). При этом наблюдалась тенденция к увеличению показателей инфицирования ВПЧ типов 16 и 18 по сравнению с другими генотипами ВПЧ у женщин в возрасте 20–29 лет. Наиболее распространенными генотипами ВПЧ, связанными с инвазивным РШМ, явились ВПЧ 16 (51%), 18 (21%), 31 (4%), 45 (3%) и 52 (3%) [16]. В 2008 г. в Новой Зеландии была внедрена Национальная программа иммунизации женщин четырехвалентной вакциной против ВПЧ (генотипы 6, 11, 16, 18). Позже, в 2013–2016 гг., выполнено исследование, показавшее снижение доли цервикальной интраэпителиальной неоплазии (CIN 2), связанной с HPV 16/18, в когорте молодых новозеландских женщин, что может быть связано с внедрением национальной программы вакцинации против ВПЧ. Это исследование имело важное значение, поскольку это первые документированные данные об изменении генотипа ВПЧ у женщин с поражениями шейки матки после начала программы вакцинации [17]. ВПЧ 16 типа является наиболее распространенным во всем мире генотипом, выявленным у пациенток с инвазивным РШМ, за ним следует ВПЧ 18 типа. Восемь генотипов ВПЧ (16, 18, 31, 33, 35, 45, 52 и 58) приводят к более высоким уровням прогрессирования РШМ [18]. В клинических рекомендациях Японского общества акушерства и гинекологии и Японской ассоциации акушеров и гинекологов представлен алгоритм ведения пациенток с CIN, который включает генотипирование ВПЧ для определения степени риска прогрессирования в CIN 3 [19]. Однако связь между генотипом ВПЧ и прогнозом развития ракового процесса остается спорной. Одни исследования показали, что ВПЧ 18-позитивные опухоли связаны с плохим прогнозом [20]. Другие авторы утверждают, что китайские и британские пациентки с опухолями, ассоциированными с ВПЧ 16 и/или 18 типа, имеют лучшую выживаемость, в то время как в Тайване получены благоприятные результаты для ВПЧ 58- и 31-положительных опухолей [21]. Напротив, иные ученые не обнаружили ассоциаций между генотипом ВПЧ и прогнозом РШМ в популяциях русских и корейцев [22]. Цитологическое исследование шейки матки, выполненное в трех медицинских учреждениях Японии, продемонстрировало, что ВПЧ 18-положительные опухоли были связаны с плохой выживаемостью женщин. Более длительное наблюдение (102 мес.) подтвердило, что ВПЧ 16-положительные опухоли коррелируют с лучшей выживаемостью по сравнению с ВПЧ 18-положительными опухолями. Эти противоречивые результаты могут быть частично обусловлены географическими различиями в распространенности типа ВПЧ [23].
Факторы, повышающие восприимчивость к ВПЧ
Микробы считаются основным триггерным фактором развития злокачественных новообразований. По данным проекта Human Microbiome (HMP) определено, что 20% всех смертельных злокачественных опухолей являются микробиологически индуцированными. Эктоцервикс колонизирован микробами, тогда как эндоцервикс и верхний генитальный тракт считаются практически стерильными у здоровых женщин. Изменения цервико-вагинального микробиома и такие процессы, как бактериальный вагиноз, воспаление шейки матки и повышение вагинального рН, влияют на восприимчивость к цервикальному ВПЧ. Женщины в разных этнических группах отличаются микробиомом влагалища [24]. Большинство цервико-вагинальных инфекций и вагинального дискомфорта обусловлены Gardnerellavaginalis
или
Atopobiumvaginae
[25], а также Candida albicans [26]. Цервикальный эпителий становится уязвимым под влиянием инфекционных микробных агентов для таких инфекций, как ВПЧ [27]. С развитием современных методик секвенирования становится понятным, что микробиом влияет на восприимчивость к раку из-за производства вредных метаболитов и их влияния на клеточную функцию, поскольку дерегулированный метаболизм и воспаление являются признаками рака [28]. Связь специфических микробов (прокариотических и эукариотических) с ВПЧ-инфекциями и цервикальной неоплазией остается одним из значимых вопросов в исследованиях. Известно, что в микробиноме здоровых женщин доминируют
Lactobacilli
. Этот константный вагинальный вид производит молочную кислоту в виде ферментации продуктов, что приводит к снижению вагинального рН до 3,5–4,5, создавая химический барьер для патогенов [29]. Высокий уровень
L. iners
связан с риском развития ВПЧ-ассоциированных цервикальных поражений. Повышение индекса массы тела коррелирует с увеличением численности
L. iners
, что делает ожирение значимым фактором развития CIN [30]. L. iners более приспособлены к изменению pH и разнообразным метаболическим состояниям, чем другие лактобациллы. Высокая обсемененность шейки матки
L. kitasatonis
и
L. crispatus
в сочетании с высокоонкогенными типами ВПЧ повышает риск развития CIN 3. Разнообразие флоры коррелирует с тяжестью CIN. Обнаружение
Sneathia sanguinegens, Anaerococcus tetradius
и
Peptostreptococcus anaerobius
у кавказских, азиатских и чернокожих женщин в микробиоме влагалища часто сочетается с развитием CIN.
P. мicros
— необычный таксон, часто встречающийся в ротовой полости, обнаруженный в слюнном микробиоме и распространенный при наличии цервикальных поражений. Выдвинуто предположение, что P. мicros может проникать в цервико-вагинальный тракт в результате орального секса [31]. Обнаружена прямая связь ВПЧ с доминированием трех грибов родов
Candida
,
Malassezia
и
Sporidiobolaceae. Malassezia
— липофильные, паразитирующие в верхних слоях кожи человека грибы, вызывающие поверхностные грибковые инфекции, такие как атопический дерматит и псориаз.
Malassezia
часто обнаруживается у мужчин на крайней плоти и головке полового члена. Malassezia производят биоактивные индолизины, включая активаторы арильного углеводородного рецептора (AhR). Рецепторы AhR опосредуют многие функции кожи, включая ускорение деления клеток, поэтому было высказано предположение, что Malasseziа могут участвовать в кожном канцерогенезе. Проведенное недавно исследование выявило, что определенная структура микробиома цервико-вагинального тракта коррелирует как с высокоонкогенными типами ПВИ, так и с CIN-тяжестью в популяции женщин репродуктивного возраста. Поэтому поиск особенностей микробиома цервико-генитальной системы может быть важным шагом в понимании биологии цервикальной неоплазии и разработке новых терапевтических схем, нацеленных на микробиоту [32].
Лечение диспластических изменений шейки матки
Поскольку CIN затрагивает в основном женщин репродуктивного возраста, имеется необходимость раннего выявления и улучшения стратегий лечения наиболее клинически значимых CIN. Персистирующая инфекция высокоонкогенными типами ВПЧ является необходимым условием прогрессирования патологии шейки матки. Первичная (вакцинация) и вторичная профилактика (скрининг шейки матки) может оказать решающее влияние на профилактику рака [32]. Поиск препаратов, направленных на лечение диспластических изменений шейки матки, — важное направление гинекологии. Йод — это антисептик, который используется в лечебной практике более 150 лет. Повидон-йод
— одно из самых мощных и эффективных йодсодержащих антисептических средств широкого спектра действия. Главное отличие этого препарата в том, что на фоне его приема не возникает резистентности микроорганизмов, он реже, чем антибиотиксодержащие препараты, вызывает аллергическую реакцию. Антисептическое действие повидон-йода связано с сильным окислительным эффектом. Под действием повидон-йода происходит образование пор в мембранах клеток микроорганизмов, что приводит к нарушению целостности клеточной оболочки, повреждению клетки и утрате ею жизнеспособности. Препарат имеет несколько преимуществ перед другими антисептиками. Во-первых, он эффективнее купирует размножение микроорганизмов даже в большом разведении. Во-вторых, у повидон-йода самый широкий противовирусный спектр действия, включающий энтеровирусы, вирусы полиомиелита и герпеса, а также аденовирусы и вирус гриппа. Повидон-йод — устойчивый препарат, его эффективность не изменяется под действием физико-химических условий в очаге воспаления, обусловленных изменением рН, белками, кровью, действием ферментов. В гинекологической практике он чаще всего используется для лечения воспалительных процессов и профилактики развития осложнений после инвазивных вмешательств [33]. Было продемонстрировано, что препарат индуцирует гибель эпителиальных клеток HeLa у крыс. Дополнительные данные, подтверждающие сильное противоопухолевое действие молекулы йода и иодолактонов, были установлены с помощью исследований клеточной культуры. Они выявили значительное снижение клеточного роста при раке молочной железы. Снижение пролиферации под действием молекул йода отмечено и в других злокачественных клеточных линиях человека (нейробластома, глиома, меланома, карциномы легких, толстой кишки и поджелудочной железы) [34]. Сравнительный анализ антипролиферативной/цитотоксической способности I2, йодида калия (KI), комбинированного раствора KI+I2, повидон-йода и I2+ [KI+глицерол] на клетках карциномы человека показал, что повидон-йод может быть потенциальным инструментом для непосредственного вмешательства в рост опухолевых клеток [35]. Рандомизированное исследование, проведенное в США, выявило, что у всех 88 обследуемых пациенток в возрасте 23–67 лет (в среднем 34,8 года) с аномальной цитологией и наличием высокоонкогенного типа ВПЧ после проведения 2 курсов криотерапии шейки матки и локального лечения повидон-йодом через 6 мес. после терапии ВПЧ не был обнаружен [36]. Исследования показали, что применение препарата
Бетадин
® после обработки кондилом раствором для наружного применения с местно-некротизирующим действием повышает эффективность лечения, снижает частоту присоединения бактериальной инфекции и рецидивирования ПВИ слизистой влагалища и шейки матки. В связи с вышеизложенным очевидна целесообразность комплексного лечения патологии шейки матки, включающего повидон-йод [37].
Заключение
Понимание особенностей персистенции ПВИ в эпителии шейки матки и связанного с ней процесса развития заболеваний данной области определяет тактику терапии повреждений шейки матки, ассоциированных с ВПЧ. Методов лечения ВПЧ гениталий много, однако частота рецидивов этого заболевания высока. Поэтому весьма перспективным направлением является разработка комплексной терапии с целью профилактики рецидивирования ВПЧ-ассоциированных заболеваний шейки матки. Применение повидон- йода (например, препарата Бетадин®) в комплексной терапии ПВИ повышает эффективность лечения, снижает частоту бактериальной инфекции, а также частоту рецидивирования ПВИ слизистой влагалища и шейки матки. Сведения об авторах:1Дубровина Светлана Олеговна — д.м.н., профессор, главный научный сотрудник Научно-исследовательского института акушерства и педиатрии; 2Красильникова Лилия Викторовна — к.м.н., акушер-гинеколог;1Ардинцева Оксана Александровна — аспирант;3Варичева Марианна Владимировна — акушер-гинеколог; 4Циркунова Нина Сергеевна — акушер-гинеколог, заведующая гинекологическим отделением;1Африкян Олег Артурович — студент 6 курса;1Афанасова Пелагея Николаевна — студентка 6 курса;5Гаджибекова Наина Балабековна — акушер-гинеколог.1ФГБОУ ВО РостГМУ Минздрава России. 344022, Россия, г. Ростов-на-Дону, пер. Нахичеванский, д. 29.2ООО «ДАВИНЧИ ГРУПП». 344091, Россия, г. Ростов-на-Дону, ул. Толмачева, д. 117.3МБУЗ «Городская больница № 20 г. Ростова-на-Дону». 344091, Россия, г. Ростов-на-Дону, пр. Коммунистический, д. 39.4МБУЗ «Городская больница № 6 г. Ростова-на-Дону». 344025, Россия, г. Ростов-на-Дону, ул. Сарьяна, д. 85/38.5МБУЗ «ГБСМП». 347930, Россия, Ростовская область, г. Таганрог, Большой просп., д. 16.Контактная информация:Ардинцева Оксана Александровна, e-mail:[email protected].Прозрачность финансовойдеятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.Конфликт интересовотсутствует.Статья поступила26.11.2018. About the authors:1Svetlana O. Dubrovina — MD, PhD, Professor, Principal Researcher of the Scientific Research Institute of Obstetrics and Pediatrics;2Liliya V. Krasilnikova — MD, PhD, obstetrician-gynecologist;1Oxana А. Ardintseva — graduate student;3Marianna V. Varicheva — obstetrician-gynecologist;4Nina S. Tsirkunova — obstetrician-gynecologist, Head of the Department of Gynecology;1Oleg A. Afrikyan — 6th year student;1Pelageya N. Afanasova — 6th year student;5Naina B. Gadzhibekova — obstetrician-gynecologist.1Rostov State Medical University. 29, per. Nakhichevanskiy, Rostov-on-Don, 344022, Russian Federation.2LLC «DAVINCI GROUP». 117, Tolmacheva sr., Rostov-on-Don, 344091, Russian Federation. 3Rostov-on-Don City Hospital No. 20. 39, Kommunisticheskiy pass., Rostov-on-Don, 344091, Russian Federation.4Rostov-on-Don City Hospital No. 6. 85/38, Saryana str., Rostov-on-Don, 344025, Russian Federation.5City Emergency Hospital. 16, Bolshoy prosp., Taganrog, Rostov region, 347930, Russian Federation.Contact information:Oxana А. Ardintseva, e-mail:[email protected].Financial Disclosure:no author has a financial or property interest in any material or method mentioned.Received26.11.2018.
Опасное солнце.
Для каждого человека критическая продолжительность воздействия солнечных лучей сугубо индивидуальна. Определить эту грань нелегко, поэтому лучше просто запомнить, что длительное пребывание на солнце идет во вред организму. Кожа вынуждена защищаться от ультрафиолетового излучения. Чрезмерный загар — это неминуемые ожоги. Если же вы настолько любите пляжный отдыха, что просто не можете отказать себе в этом удовольствии, прислушайтесь хотя бы к следующим советам. Соблюдая эти несложные рекомендации, вы не только укрепите здоровье, но и снизите риск опасного заболевания.
- Пребывание на солнце безопасно с утра до 10 часов, вечером после 17 часов.
- Людям с большим количеством родинок пребывание на солнце лучше сократить.
- Постарайтесь не допускать покраснений и солнечных ожогов на коже. Если это произошло, 2-3 дня проведите в тени.
- После купания в море обязательно ополосните кожу пресной водой.
- Даже молодым и здоровым людям находиться на солнце можно не более полутора- двух часов в день.
- Прием определенных лекарств повышает светочувствительность кожи. Перед отпуском проконсультируйтесь со своим терапевтом.
- Используйте солнцезащитную косметику: в начале отпуска показатель должен быть максимальным, около 40 единиц.
- Не пользуйтесь на пляже декоративной косметикой, дезодорантами и духами — они могут спровоцировать появление пигментных пятен на коже.
«Удалять родинки или нет?»
Есть образования на коже, которые удалять необходимо, потому что есть высокий риск возникновения онкологического заболевания.
Преимущественно подобные образования иссекаются с обязательным гистологическим исследованием операционного материала. Доброкачественные, не предраковые образования кожи подлежат удалению по косметическим показаниям, в случае неприятных ощущений (травматизация, зуд), если происходит постоянное повреждение образования или иной дискомфорт.
В любом случае о том, нужно ли удалять родинки необходимо проконсультироваться с врачом дерматологом, онкологом. Он же должен порекомендовать оптимальный метод удаления.
Сколько заживает рана после лазерного удаления
Длительность периода полного заживления зависит от многих факторов:
- от самой структуры ткани, например слизистая восстанавливается быстрее, чем грубая толстая кожа на стопе или ладонях;
- от интенсивности кровоснабжения участка на котором было удаление, хорошо кровоснабжаемые участки в 2 раза быстрее заживают, чем например пятки и стопа, где кровоток в поверхностных слоях дермы практически отсутствует;
- от размера раны, которая образовалась после удаления, небольшие по диаметру дефекты заживают в 3 раза быстрее.
Уже в конце первых суток по периферии раны увеличивается количество клеток участвующие в регенерации (для сравнения при других методах воздействия только к концу 3-х). К 5-7 отмечается активный процесс ангиогенеза, прорастания новых сосудов. И к 14-20 дня полностью восстанавливается структура ткани без образования рубцовых изменений.
Какие виды кератом существуют
Кератомы бывают нескольких видов:
- себорейная;
- возрастная;
- сенильная;
- роговая;
- солнечная;
- фолликулярная.
Себорейная кератома — крайне неприятное кожное заболевание. На вид это небольшие пятна желтого или коричневого цвета, однако они имеют свойство увеличиваться в размере со временем, покрываться трещинами, грубеть. Может возникать чувство зуда и жжения, а также кровоточивость и болезненность пораженных участков эпителия.
Старческие кератомы образуются у людей пожилого возраста. Они имеют желтоватый или коричневый окрас, а в диаметре могут достигать 5–6 сантиметров. Возрастные кератомы обычно выпуклые, ощущаются над кожей. Они могут иметь неровную поверхность, как бы покрытую ямками, походящую на наперсток. Чаще всего эти кожные наросты образуются на шее, лице и руках.
Сенильная кератома обычно появляется у людей в возрасте старше 30 лет. Она покрывается корочкой сероватого цвета. Доброкачественное новообразование подвержено постоянным воспалительным процессам и кровоточивости.
Рекомендуемые статьи по теме:
- Ультразвуковой пилинг кожи лица – приятная и полезная процедура для вашей кожи
- Редермализация кожи: все «за» и «против»
- Миндальный пилинг для лица: особенности процедуры
Роговая кератома носит такое название, потому что напоминает на вид рог животного. Обычно этот вариант кожного заболевания является запущенной формой кератомы возрастного или себорейного типов.
Солнечная кератома поражает тех, кто любит злоупотреблять загаром или посещением солярия. Она образуется на участках кожи, которые наиболее подвержены воздействию ультрафиолета — лице, руках, плечах, груди. Кератома окрашена в серый, желтый или коричневый цвет.
Фолликулярная кератома появляется на участках кожи, покрытых волосами (голова, лицо). Она похожа на узелок, окрашенный в серый цвет и достигающий 1,5 сантиметров в диаметре. Это наиболее редкий тип кератомы.