Статья на конкурс «Био/Мол/Текст»: Акне, или в просторечии прыщи, по приблизительным оценкам есть у 70% людей и почти 85% подростков. Акне — сложное многофакторное заболевание, и нам стало интересно, какую роль в нем играют микроорганизмы, обитающие на коже. Известно, что у еще не родившегося ребенка кожа стерильна, но вскоре после рождения она колонизируется разнообразными микроорганизмами окружающей среды. Они и формируют микробиом наших внешних покровов. Мы решили подробно рассмотреть, ладят ли бактерии и кожа, какие отношения формируются между бактериями — и как на это влияет генетика и среда.
Конкурс «Био/Мол/Текст»-2021/2022
Эта работа опубликована в номинации «Школьная» конкурса «Био/Мол/Текст»-2021/2022.
Партнер номинации — некоммерческая школа-пансион «Летово».
Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.
Генеральный партнер конкурса — : крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Строение кожи
Кожа человека состоит из трех слоев (рис. 1).
Гиподерма, или подкожно-жировая клетчатка, — самый глубокий слой. Это главное хранилище жира в организме.
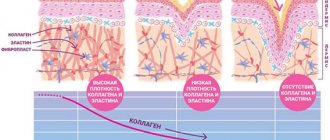
Дерма (или собственно кожа) располагается между эпидермисом и гиподермой. Она представляет собой соединительную ткань с многочисленными волокнами коллагена и эластина. Во многом определяет состояние кожи — увлажненность и упругость.
Дерма контактирует с базальным слоем, который дает начало верхнему слою — эпидермису. Основные клетки эпидермиса — кератиноциты. Они по мере своего роста двигаются от базальной мембраны вверх, выделяя липиды. Выделяют несколько слоев кератиноцитов — в зависимости от возраста и состояния клеток, которые сменяются примерно за месяц [1].
Мы еще не упомянули о производных эпидермиса. Сальные, потовые, серные и молочные железы, волосы имеют с ним одно происхождение. Сальные железы выделяют кожное сало (себум), которым с удовольствием питаются микроорганизмы.
Кожа — отдельная экологическая ниша, в которой формируются сложные микробные сообщества. Совокупность населяющих кожу микроорганизмов, или микробиом, — динамичная система со своими закономерностями. Тут, как и в любой экосистеме, между организмами существуют разные связи. А также микроорганизмы взаимодействуют со средой, которая во многом диктует условия их существования [2].
Рисунок 1А. Строение кожи.
Рисунок 1Б. Строение эпидермиса.
авторский рисунок
Рисунок 1В. Строение сальной железы.
Теперь поговорим про кожный барьер. Это система из разнообразных липидов и кератиноцитов, защищающая кожу от обезвоживания и механических повреждений. Но в рамках статьи нас интересует, что кожный барьер нужен для предотвращения воздействия бактерий и патогенов на жизнедеятельность клеток кожи [3].
Кожный барьер принято разделять на две составляющие — гидролипидную мантию и липидо-эпидермальный барьер (рис. 2). Главная функциональная особенность гидролипидной мантии, состоящей в основном из выделений сальных и потовых желез, — кислая среда, pH примерно от 4,7 до 5,7. Благодаря ей перестают размножаться и погибают вредоносные бактерии. Липидо-эпидермальный барьер представляет из себя множество мертвых клеток, скрепленных между собой липидами, которые они по мере взросления постепенно выделяли во внешнюю среду. Именно он защищает кожу от обезвоживания, снижая трансэпидермальную потерю влаги (ТЭПВ), а также является вторым звеном защиты после гидролипидной мантии от проникновения в кожу бактерий и аллергенов.
Однако не стоит считать, что кожный барьер полностью защищает нас от патогенов. При исследованиях все же было обнаружено присутствие бактерий в дерме и гиподерме [4].
Рисунок 2. Кожный барьер не защищает кожу от проникновения бактерий полностью. Кератиноциты по мере роста выделяют многочисленные пластины, содержащие липиды (кератиносомы). Благодаря межклеточным связкам — корнеодесмосомам — и липидам, корнеоциты, то есть мертвые клетки рогового слоя эпидермиса, скрепляются между собой, формируя цельную структуру, и увлажняются NMF — натуральным увлажняющим фактором. Это молекулы, которые помогают удержать больше воды в эпидермисе: свободные аминокислоты, мочевина, лактаты и др.
сайт
Дерма
Дерма представляет собой сложноорганизованную рыхлую соединительную ткань, состоящую из отдельных волокон, клеток, сети сосудов и нервных окончаний, а также эпидермальных выростов, окружающих волосяные фолликулы и сальные железы. Клеточные элементы дермы представлены фибробластами, макрофагами и тучными клетками. Лимфоциты, лейкоциты и другие клетки способны мигрировать в дерму в ответ на различные стимулы.
Дерма, составляя основной объем кожи, выполняет преимущественно трофическую и опорную функции, обеспечивая коже такие механические свойства, как пластичность, эластичность и прочность, необходимые ей для защиты внутренних органов тела от механических повреждений. Также дерма удерживает воду, участвует в терморегуляции и содержит механорецепторы. И, наконец, ее взаимодействие с эпидермисом поддерживает нормальное функционирование этих слоев кожи.
В дерме нет такого направленного и структурированного процесса клеточной дифференцировки, как в эпидермисе, тем не менее в ней также прослеживается четкая структурная организация элементов в зависимости от глубины их залегания. И клетки, и внеклеточный матрикс дермы также подвергаются постоянному обновлению и ремоделированию.
Внеклеточный матрикс (ВКМ) дермы, или межклеточное вещество, в состав которого входят различные белки (главным образом коллаген, эластин), гликозаминогликаны, самым известным из которых является гиалуроновая кислота, и протеогликаны (фибронектин, ламинин, декорин, версикан, фибриллин). Все эти вещества секретируются фибробластами дермы. ВКМ представляет собой не беспорядочное скопление всех компонентов, а сложноорганизованную сеть, состав и архитектоника которой определяют такие биомеханические свойства кожи, как жесткость, растяжимость и упругость. К белкам ВКМ прикрепляются кератиноциты эпидермиса, которые тесно состыкованы друг с другом. Именно они и формируют плотный защитный слой кожи. Структура ВКМ также способна оказывать регулирующее влияние на погруженные в него клетки. Регуляция может быть как прямой, так и косвенной. В первом случае белки и гликозаминогликаны ВКМ непосредственно взаимодействуют с рецепторами клеток и инициируют в них специфические пути передачи сигнала. Косвенная регуляция осуществляется посредством действия цитокинов и ростовых факторов, удерживаемых в ячейках сети ВКМ и высвобождаемых в определенный момент для взаимодействия с рецепторами клеток. Структурная сеть ВКМ подвергается ремоделированию ферментами из семейства матриксных металлопротеиназ (ММР). В частности, ММР-1 и ММР-13 инициируют деградацию коллагенов I и III типов. Плотность сети ВКМ дермы неравномерна – в папиллярном слое она более рыхлая, в ретикулярном — значительно плотнее как за счет более близкого расположения волокон структурных белков, так и за счет увеличения диаметра этих волокон.
Коллаген – один из главных компонентов ВКМ дермы. Синтезируется фибробластами. Процесс его биосинтеза сложный и многоступенчатый, в результате которого фибробласт секретирует в экстрацеллюлярное пространство проколлаген, состоящий из трех полипептидных α-цепей, свернутых в одну тройную спираль. Затем мономеры проколлагена ферментивным путем собираются в протяженные фибриллярные структуры различного типа. Всего в коже не менее 15 типов коллагена, в дерме больше всего I, III и V типов этого белка: 88, 10 и 2% соответственно. Коллаген IV типа локализуется в зоне базальной мембраны, а коллаген VII типа, секретируемый кератиноцитами, играет роль адаптерного белка для закрепления фибрилл ВКМ на базальной мембране (рис. 4). Волокна структурных коллагенов I, III и V типов служат каркасом, к которому присоединяются другие белки ВКМ, в частности коллагены XII и XIV типов. Считается, что эти минорные коллагены, а также небольшие протеогликаны (декорин, фибромодулин и люмикан) регулируют формирование структурных коллагеновых волокон, их диаметр и плотность образуемой сети. Взаимодействие олигомерных и полимерных комплексов коллагена с другими белками, полисахаридами ВКМ, разнообразными факторами роста и цитокинами приводит к образованию особой сети, обладающей определенной биологической активностью, стабильностью и биофизическими характеристиками, важными для нормального функционирования кожи. В папиллярном слое дермы волокна коллагена располагаются рыхло и более свободно, тогда как ее ретикулярный слой содержит более крупные тяжи коллагеновых волокон.
Рис. 4. Схематичное представление слоев кожи и распределения коллагенов разных типов.
Коллаген постоянно обновляется, деградируя под действием протеолитических ферментов коллагеназ и замещаясь вновь синтезированными волокнами. Этот белок составляет 70% сухого веса кожи. Именно коллагеновые волокна «держат удар» при механическом воздействии на нее.
Эластин формирует еще одну сеть волокон в дерме, наделяя кожу такими качествами, как упругость и эластичность. По сравнению с коллагеном эластиновые волокна менее жесткие, они скручиваются вокруг коллагеновых волокон. Именно с эластиновыми волокнами связываются такие белки, как фибулины и фибриллины, с которыми, в свою очередь, связывается латентный TGF-β-связывающий белок (LTBP). Диссоциация этого комплекса приводит к высвобождению и к активации TGF-β, самого мощного из всех факторов роста. Он контролирует экспрессию, отложение и распределение коллагенов и других матриксных белков кожи. Таким образом, интактная сеть из волокон эластина служит депо для TGF-β.
Гиалуроновая кислота (ГК) представляет собой линейный полисахарид, состоящий из повторяющихся димеров D-глюкуроновой кислоты и N-ацетилглюкозамина. Количество димеров в полимере варьирует, что приводит к образованию молекул ГК разного молекулярного веса и длины — 1х105-107 Да (2-25 мкм), оказывающих, соответственно, различный биологический эффект.
ГК — высокогидрофильное вещество, влияющее на движение и распределение воды в матриксе дермы. Благодаря этому ее свойству наша кожа в норме и в молодости обладает высоким тургором и сопротивляемостью механическому давлению.
ГК с легкостью образует вторичные водородные связи и внутри одной молекулы, и между соседними молекулами. В первом случае они обеспечивают формирование относительно жестких спиральных структур. Во втором – происходит ассоциация с другими молекулами ГК и неспецифическое взаимодействие с клеточными мембранами, что приводит к образованию сети из полимеров полисахаридов с включенными в нее фибробластами. На длинную молекулу ГК, как на нить, «усаживаются» более короткие молекулы протеогликанов (версикана, люмикана, декорина и др.), формируя агрегаты огромных размеров. Протяженные во всех направлениях, они создают каркас, внося вклад в стабилизацию белковой сети ВКМ и фиксируя фибробласты в определенном окружении матрикса. В совокупности все эти свойства ГК наделяют матрикс определенными химическими характеристиками – вязкостью, плотностью «ячеек» и стабильностью. Однако сеть ВКМ является динамической структурой, зависящей от состояния организма. Например, в условиях воспаления агрегаты ГК с протеогликанами диссоциируют, а образование новых агрегатов между вновь синтезированными молекулами ГК (обновляющимися каждые 3 дня) и протеогликанами блокируется. Это приводит к изменению пространственной структуры матрикса: увеличивается размер его ячеек, меняется распределение всех волокон, структура становится более рыхлой, клетки меняют свою форму и функциональную активность. Все это сказывается на состоянии кожи, приводя к снижению ее тонуса.
Помимо регуляции водного баланса и стабилизации ВКМ, ГК выполняет важную регуляторную роль в поддержании эпидермального и дермального гомеостаза. ГК активно регулирует динамические процессы в эпидермисе, включая пролиферацию и дифференцировку кератиноцитов, окислительный стресс и воспалительный ответ, поддержание эпидермального барьера и заживление раны. В дерме ГК также регулирует активность фибробластов и синтез коллагена. Ремоделируя матрикс, ГК управляет функционированием клеток в матриксе, влияя на их доступность для различных факторов роста и изменяя их функциональную активности. От действия ГК зависит миграция клеток и иммунный ответ в ткани. Таким образом, изменения в распределении, организации, молекулярном весе и метаболизме ГК имеют значимые физиологические последствия.
Фибробласты представляют собой основной тип клеточных элементов дермы. Именно эти клетки отвечают за продукцию ГК, коллагена, эластина, фибронектина и многих других белков межклеточного матрикса, необходимых для формирования соединительной ткани. Фибробласты в различных слоях дермы различаются и морфологически, и функционально. От глубины их залегания в дерме зависит не только количество синтезируемого ими коллагена, но и соотношение типов этого коллагена, например I и III типов, а также синтез коллагеназы: фибробласты более глубоких слоев дермы производят меньшее ее количество. Вообще, фибробласты – очень пластичные клетки, способные менять свои функции и физиологический ответ и даже дифференцироваться в другой тип клеток в зависимости от полученного стимула. В роли последнего могут выступать и сигнальные молекулы, синтезированные соседними клетками, и перестройка окружающего ВКМ.
Патогенез акне
Основной механизм возникновения акне — увеличение выработки кожного сала и количества дифференцирующихся кератиноцитов под действием андрогенов. В результате закупориваются поры, возникает анаэробная среда, и агрессивные штаммы P. acnes начинают активно размножаться. Это рано или поздно замечает наш организм, запускаются сложные воспалительные механизмы, и возникает акне [5].
Но не все так просто: акне, как уже говорилось, многофакторная болезнь, и факторов, которые могут запустить ее, довольно много:
- Генетические особенности. Выделяют несколько наследственных форм акне. Например, связанные с геном АR (андрогенный рецептор). Иногда акне связано не с избытком андрогенов, а с гиперчувствительностью рецепторов андрогенов.
- Нейроэндокринные нарушения.
- Питание.
- Избыток йода и брома, витамина B12[5].
- Некоторые лекарства и химические вещества (известно около 210).
- Применение антибиотиков широкого спектра действия. (Раньше так могли лечить акне). Они действовали против бактерий, но не против грибов рода Malassezia, выделения которых также раздражают сальные железы [5].
- Курение.
- Стресс [5]. Хотя часто сам факт наличия акне и невозможности избавиться от него являются стрессом.
- Фотоповреждение.
- Неправильно подобранная косметика.
Как уход может влиять на состояние кожи?
Поверхность здоровой кожи имеет слабокислую среду. Под воздействием косметики pH изменяется, что меняет условия жизни микрофлоры, а также может нарушить эпидермальный барьер.
Значительная часть средств для умывания защелачивают поверхность кожи. Липиды кожного барьера просто вымываются. Можно пользоваться кислым тоником, чтобы минимизировать изменения. Но не все про это знают, и не все тоники имеют подходящий pH. При целостном эпидермальном барьере кожа может восстановить баланс за пару часов, и сильного вреда разовое воздействие не приносит.
Есть и более жесткие по отношению к микробиому средства. Например, химические пилинги — популярная косметологическая процедура. Ее суть сводится к тому, что убирается верхний слой клеток эпидермиса, и кожа становится более гладкой. Однако вместе с этими клетками уходит и множество бактерий, что уменьшает их видовое разнообразие. А разнообразие — часто признак хорошего микробиома. Также пилинг чрезмерно понижает pH кожи.
Почему это важно знать?
Многие массовые косметические средства, направленные на лечение акне, могут, наоборот, навредить вашей коже. Поэтому важно тщательно подбирать косметику для домашнего использования [6]. Ведь при систематическом нарушении целостности эпидермального барьера кожа становится более уязвимой к различным внешним воздействиям, возрастает трансэпидермальная потеря влаги. Это плохо сказывается как на внешнем виде, так и на здоровье.
Рисунок 3. Распределение семейств бактерий на коже человека. В таблице внизу под разными цветами указаны названия семейств бактерий; им соответствуют цвета в диаграммах на основной схеме. Рядом с диаграммами — разноцветные точки: синие — зоны с повышенным производством себума, зеленые — влажные, красные — сухие.
[7]
Факторы риска
Этиология пиодермии не ограничивается механизмами образования гнойно-воспалительного процесса. Дерматологам известны формы предрасположенности к этому заболеванию, связанные с образом жизни, наследственностью и индивидуальным анамнезом пациента.
Известные факторы риска:
- Несоблюдение правил личной гигиены. Постоянное загрязнение кожи увеличивает риск инфекции.
- Перегревание или переохлаждение покровных тканей. Перепады температуры нарушают функции местного иммунитета. Зачастую после переохлаждения кожный покров становится воротами инфекции.
- Возраст. У новорожденных и пожилых людей чаще всего возникает пиодермия из-за недостаточной эффективности местного иммунитета.
- Наличие большого количества аллергических реакций и аутоиммунных заболеваний (особенно у ребенка.)
- Патологии эндокринной системы. Состояние кожи в значительной степени зависит от гормональных влияний.
- Заболевания обмена веществ: сахарный диабет и ожирение.
- Врожденные и приобретенные иммунодефицитные состояния.
- Неправильное питание, приводящее к дефициту определенных витаминов и микроэлементов в организме.
- Неблагоприятная семейная наследственность. Кожные заболевания могут быть связаны с передачей генетических мутаций.
Возбудители пиодермического дерматита находятся в окружающей среде и на поверхности покровных тканей. Это стафилококки, стрептококки и некоторые патогенные грибки. Часто люди заражаются гноеродными бактериями в больничных условиях.
Микробиом кожи
Карта. Кто где живет
Давайте рассмотрим наиболее распространенные микроорганизмы и места их обитания на коже. Те из них, кто живет в одном месте на теле, оказывают друг на друга наибольшее влияние.
P. acnes и P. granulosum обнаруживаются в областях, богатых сальными железами. P. acnes преобладает на коже головы, лба, ушей, на спине и крыльях носа. Это основной колонизатор сальных желез.
Влажные области, такие как пупок или подмышечная впадина, в основном содержат виды Staphylococcus и Corynebacteria. Подмышечная область заселена грамположительными бактериями родов Staphylococcus, Micrococcus, Corynebacterium а также некоторыми Propionibacterium (рис. 3) [7].
В более сухих местах обитают преимущественно Staphylococcus, Micrococcus, Corynebacterium, Enhydrobacter и Streptococcus
Возможно, упомянутое нами ранее название P. acnes натолкнуло вас на мысль, что именно эти бактерии и вызывают акне.
Прежде всего следует вспомнить, что акне — это сложное и многофакторное заболевание, которое не может зависеть от одной бактерии. Некоторые исследования даже показывают, что здоровые кожные фолликулы представляют собой среду обитания, допускающую заселение только P. acnes, тогда как у пациентов с акне обнаружили Staphylococcus epidermidis и другие виды. Поэтому роль P. acnes достаточно неоднозначна, и есть даже вероятность, что P. acnes не вызывают акне, а наоборот, защищают от него [8].
Мнение о том, что кожа — место обитания только для бактерий, ошибочно. На самом деле, микробиом наших покровов гораздо разнообразнее и включает в состав различные виды протистов, грибов, а иногда даже животных типа Членистоногие! Ниже вы можете видеть кожного клеща демодекс — типичного обитателя кожи человека, питающегося в основном кожным салом. Этот товарищ сам по себе безобиден, но его чрезмерное размножение у некоторых людей может вызвать аллергическую реакцию, проявляющуюся в виде акнеподобного состояния (маленьких прыщиков).
Видео 1. Это — кожный клещ. У каждого человека живет по крайней мере один вид.
Какие бывают кожные болезни у человека?
Кожные заболевания могут быть различного происхождения. Все они отличаются своим видом, симптомами и причиной образования.
Самые распространенные из них:
- Грибки. Грибковые заболевания кожного покрова у человека, как правило, вызывают грибки-паразиты, чье происхождение является растительным. Такие заболевания обычно поражают: ногтевую пластину, волосы, кожный покров. Грибковые заболевания являются заразным, значит они легко могут передаваться от одного организма к другому.
- Гнойники. Провокаторами гнойничковых заболеваний кожи являются стафилококки и стрептококки. Также причиной образования гнойников могут стать инфекции в качестве последствия охлаждения и психической травмы. Гнойничковые заболевания кожи делятся на два основных вида: поверхностная пиодермия и глубокая пиодермия.
- Заболевания кожи, которые вызваны животными паразитами. К таким болезням относятся: педикулез и чесотка. Первый достаточно просто вылечить. Возбудителем чесотки, как правило, является чесоточный зудень или клещ. При первых же симптомах чесотки необходимо начать лечение, так как, в противном случае, это может привести к образованию экземы.
- Лишаи. Лишаи имеют несколько видов. Самые распространенные из них: розовый лишай, плоский красный лишай, опоясывающий лишай, цветной лишай. У каждого вида есть свои особенности и причины образования.
- Заболевания кожных желез. Самыми распространенными видами этих заболеваний являются: себорея и угри. Если себорея поражает голову, то начинается выпадение волос. Угри чаще всего проявляются в молодом возрасте, чаще всего на основе себореи.
Как бактерии приспособились жить на коже
Микробиом кожи формируется под влиянием большого разнообразия переменных: возраст, пигментация кожи, факторы среды (солнечные лучи, косметика, которой мы постоянно пользуемся) [7], [9], [10].
Распределение видов на поверхности мы уже рассмотрели, копнем вглубь. Выявлено, что нижняя часть блестящего слоя эпидермиса (рис. 1) имеет щелочную реакцию, средняя — нейтральную, и уже мертвые клетки — кислую [1]. Таким образом, условия среды зависят не только от места на теле, но и от глубины, на которой бактерии заселяют кожу.
Все организмы стремятся увеличивать свою численность, и бактерии не исключение. Вот часть выработанных ими успешных стратегий:
- Изменчивые белки. Бактерии одного вида отличаются друг от друга, и иммунитет хуже опознает и расправляется с ними.
- Белки, обеспечивающие прикрепление к эпителию. Чем лучше бактерии закрепятся на эпидермисе, тем больше будет этого вида [11].
- Вещества, которые мешают жить конкурентам: антибиотики, SCFAs (короткоцепочечные жирные кислоты), и так далее [12].
- Вещества, которые действует против других штаммов того же вида [13].
Ряд SCFAs естественным образом продуцируется клетками кожи, а также полезными бактериями, которые тоже научились расщеплять жирные кислоты до более коротких фрагментов. Такие бактерии помогают коже выполнять ее защитную функцию, так как SCFAs замедляют развитие случайных микроорганизмов (полезным бактериям же эта способность нужна по большей части для того, чтобы укорениться на коже). В нашем случае, P. acnes ферментируют глицерин до различных SCFAs, включая пропионовую кислоту [12].
Симптомы
Внешние проявления пиодермии зависят от глубины поражения кожного покрова, возбудителя инфекции и других факторов. Многие дерматиты проявляются сразу несколькими видами кожных образований. Дополнительные симптомы могут быть обусловлены первопричиной патологии и влиянием бактериальных токсинов на организм.
Симптомы интоксикации организма:
- головокружение и слабость;
- тошнота и рвота;
- нарушение сна;
- повышение температуры тела;
- снижение аппетита;
- головные боли;
- озноб.
При появлении перечисленных выше симптомов следует сразу же обратиться к врачу. Инфекция, вызвавшая пиодермию, может распространяться через кровь и повреждать внутренние органы. Самостоятельное удаление кожных образований увеличивает риск возникновения сепсиса.
Ладят ли бактерии и наш иммунитет?
Бактерии могут активировать различные сигнальные пути в клетках кожи человека (рис. 4).
Рисунок 4. Действие микроорганизмов может быть позитивным, негативным или нейтральным. Примером отношений между бактериями и кожей может служить врожденная способность кожи определять микроорганизмы с помощью Toll-подобных рецепторов (TLRs). Другие типы взаимодействий показаны на рисунке: вверху — влияние обычных бактерий кожи, внизу — патогенных. На цветном фоне — описания молекул. Схема довольно условная и реальных взаимодействий гораздо больше. И они сложнее.
авторский рисунок
Бактерии способны влиять на врожденный иммунный ответ кератиноцитов, делая их более или менее реактивными [14].
Лечение
Как правило, кожные заболевания лечатся следующими способами:
- Соблюдение диеты и правильного режима питания, употребление необходимых витаминов.
- Лечение лекарственными препаратами, чтобы повысить иммунную систему.
- Употребление антибиотиков, если кожное заболевание приняло тяжелую форму.
- Наружное лечение с помощью мазей и кремов.
Здесь вы можете подробно прочитать чем лечить грибок на ногах.
Связаны ли микробиом и акне?
Мы уже поняли, что на коже обитают различные бактерии, которые могут быть как полезными, так и патогенными. Теперь же следует рассмотреть их связь с акне.
Итак, бактерии и грибы колонизируют кожу потому, что для них это удобная среда обитания, так как в ней есть подходящий источник пищи — например, какой-нибудь вид эпидермальных липидов. И тут мы подходим к крайне интересному моменту. Этот липид выделился на поверхность из клетки под контролем генов. В итоге: что есть истинная причина акне — патогенная бактерия или гены? Влияние генов или среды (т. е. сформировавшегося микробиома)?
Р. acnes — полезна или вредна для здоровья?
Ранее мы уже упоминали P. acnes и обещали разобраться с ней подробнее. В этой части статьи мы поговорим о полезных и вредных чертах, различных взаимодействиях этой бактерии, а также возможности определения ее на себе.
Полезные черты
Р. acnes имеет общие свойства с молочными пропионибактериями, которые считаются безвредными — и даже полезными [12]. Подобные ей организмы обладают множеством положительных свойств: синтез витамина B12, рибофлавина, фолиевой кислоты. P. acnes также способна регулировать число других бактерий, производя SCFAs (короткоцепочечные жирные кислоты). Ферментация глицерина с помощью P. acnes и S. epidermidis может подавлять рост наиболее распространенного патогенного микроорганизма кожи Staphylococcus aureus. Это препятствует колонизации опасной бактерией кожных ран [15].
Условно-патогенные черты
Патогенезом акне называют механизм развития болезни, в котором P. acnes играет значительную роль. Она секретирует ферменты, разрушающие компоненты ткани человека, и может усугублять ряд других заболеваний [16], [17].
Закупоренная сальная железа создает анаэробную среду. Она благоприятна для P. acnes и способствует чрезмерному росту. Но при развитии акне там обнаруживали не только эту бактерию, но и другие микроорганизмы, в том числе S. epidermis. То есть в процесс вовлечена точно не одна P. acnes.
Взаимоотношения бактерий неоднозначны. S. epidermidis расщепляет жирные кислоты до более коротких SCFA. Получается, что она может сдерживать чрезмерный рост P. acnes и косвенно улучшать ситуацию с угрями [18]. Хотя не так давно мы говорили о том, что S. epidermidis и P. acnes вместе «защищают» нас от Staphylococcus aureus (золотистого стафилококка).
Взаимодействие между P. acnes и другими бактериями
P. acnes и родственные ей виды могут продуцировать бактериоцины (вещества, которые вызывают повреждение структур бактериальной клетки). Они обычно действуют против близкородственных видов, но по крайней мере один из них (пропионицин) подавляет даже некоторые грамотрицательные бактерии и грибы. К тому же P. acnes способна производить 2 вида тиопептидных антибиотиков (с высоким содержанием серы). Они сильно угнетают синтез белка у грамположительных бактерий. А некоторые штаммы P. acnes способны подавлять другие штаммы своего же вида! [13]
Бактериоцины и бактериоциноподобные вещества P. acnes могут быть ответственны за успешную конкуренцию с другими микроорганизмами, что объясняет ее доминирующее присутствие в здоровых фолликулах.
Взаимодействие между P. acnes и клетками кожи
Как еще объяснить доминирование P. acnes? У нее выявлено 4 белка, способных вызвать иммунный ответ организма. Некоторые из них изменчивы (DsA1 и DsA2). Получается, что в рамках одного вида бактерии немного отличаются, как бы маскируются. Так P. acnes уклоняется от иммунитета.
Внутри кератиноцитов есть рецепторы TLR9, которые способны улавливать бактериальную ДНК. Когда с ними связывается P. acnes, происходит очень интересная вещь: на бактерию как бы закрывают глаза и она, таким образом, может существовать внутри клетки в течение нескольких недель. После чего все-таки запускается воспаление [19].
Что происходит на здоровой коже и коже с акне?
Посмотрев на белки, можно довольно точно сказать, по какой «программе развития» пошла клетка. Так вот, в сальных железах здоровой кожи много белков, которые участвуют в защите от клеточных стрессов и активных форм кислорода.
Однако сальные железы людей с акне обнаружили белки, которые участвуют в восстановлении тканей. Это показывает, что что-то пошло не так и ткань была повреждена. Идентифицированные чужеродные белки были исключительно из P. acnes. Самые распространенные — факторы CAMP (про них — в следующем разделе), а также белки, обеспечивающие прикрепление бактерий к эпителию.
Казалось бы, все вполне ясно: P. acnes в данном случае ведет себя как агрессор. Но не тут-то было! Оказывается, эти же белки P. acnes обнаруживают и на здоровой коже. Это еще раз подтверждает неоднозначную роль P. acnes в развитии акне [11].
Диагностика
Для прохождения обследования необходимо записаться на прием к дерматологу. Врач расспросит пациента о жалобах и изучит анамнестические данные для выявления факторов риска болезни. Следующим этапом диагностики является первичный осмотр поврежденной кожи. Дерматолог оценивает форму и размер гнойников, а также определяет глубину повреждения тканей. Для уточнения причины возникновения пиодермии и тяжести состояния пациента назначаются инструментальные и лабораторные обследования.
Дополнительные методы диагностики:
- Дерматоскопия – метод визуального обследования очагов повреждения тканей. Для определения типа болезни врач использует оптический или цифровой аппарат, позволяющий многократно увеличивать изображение (фото). Дерматоскопия используется для поиска специфических признаков разных видов пиодермии и дифференциальной диагностики.
- Микробиологическое исследование содержимого пузырей, фурункулов и других патологических структур. Врач осторожно прокалывает оболочку пузыря и собирает экссудат в стерильную емкость. В лаборатории специалисты проводят посев материала на различные питательные среды для идентификации возбудителя болезни. После уточнения типа возбудителя дерматита специалисты проводят тест на чувствительность микроорганизмов к антибиотикам. Бактериальный посев является наиболее надежным способом диагностики инфекционной формы недуга.
- Анализ крови. В процедурном кабинете медсестра производит забор венозной крови и отправляет материал в лабораторию. В первую очередь специалисты оценивают соотношение и количество форменных элементов крови. Иммунологический тест позволяет обнаружить признаки аутоиммунного заболевания. Также при необходимости проводится серологическая диагностика: специалисты ищут в крови специфические антитела, вырабатываемые организмом в ответ на инфекцию. Часто требуется исключение венерической инфекции.
При неспецифических симптомах врачу необходимо исключить наличие других заболеваний с похожей симптоматикой. Для этого проводится дифференциальная диагностика токсидермии, буллёзного эпидермолиза, вегетирующей пузырчатки и грибкового поражения кожи. Исключается наличие ВИЧ-инфекции. При необходимости назначается консультация иммунолога, аллерголога, ревматолога и врача-инфекциониста.
Метаболическая активность P. acnes
Участие в воспалении
Ряд исследований in vitro показал, что определенные штаммы P. acnes умеют запускать воспаление в клетках кожи через разные механизмы [19-22], в то время как другие штаммы связаны со здоровой кожей [23], [24]. Анализ генома P. acnes выявил предполагаемые различия между ними, которые помогут объяснить ее двоякую роль [25].
Понятно, что есть и белки, которые кодируются в геномах всех P. acnes, например, факторы CAMP (Christie-Atkins-Munch-Peterson) (всего их 5). Доказано, что ингибирование CAMP2 ослабляет воспаление на модели уха мыши. Их точная роль in vivo не выяснена, но, видимо, они достаточно важны, раз сохраняются у всех P. acnes.
Профилактика
Самостоятельное предотвращение инфекционных и воспалительных заболеваний кожи не является сложной задачей.
Основные методы профилактики:
- гигиенический уход за кожей;
- своевременная обработка порезов и ожогов;
- лечение хронических инфекций;
- регулярные обследования у дерматолога при хронических кожных заболеваниях;
- контроль уровня сахара в крови при диабете.
Консультация дерматолога и иммунолога поможет пациенту узнать больше о методах профилактики и лечения пиодермии.
Выводы
Разнообразие микроорганизмов на нашем теле огромно. Можно представить кожу как гигантскую страну, население которой постоянно меняется под влиянием внешнего мира, иммунной системы и взаимодействия с соседними странами. То есть с микробиомом поверхности глаз, кишечника, слизистых. Совокупность геномов и метаболических путей некоторых микробных симбионтов может работать во благо нашего организма [26], ведь некоторые бактерии способны осуществлять полезные для человека реакции. Таких представителей микробиома можно оценивать как еще один орган человека [27].
Изменения внутри нашего организма корректируют условия жизни бактерий. Так, при повышенной секреции кожного сала происходят изменения его качественного состава.
Микробиом — сложная динамическая система. Если мы более полно охарактеризуем взаимоотношения внутри него, это может дать дополнительный взгляд на современную эволюцию человека. Поможет оценить, влияют ли — и как — развивающиеся технологии, изменения в образе жизни на здоровье и предрасположенность к заболеваниям. В частности, к акне.
Сейчас точно известно, что количественные и качественные изменения микробиома осложняют течение акне. Считается, что выделения P. acnes содержат несколько белков, которые могут провоцировать воспаление. Однако, поскольку акне — многофакторное заболевание, стоит принимать во внимание другие причины, такие как уход, генетика, стресс, питание и др. К тому же, P. acnes имеет ряд полезных черт: «защищает» нас от S. aureus, выступая в роли пробиотика. Так что некорректно винить во всем ее.
Стали появляться исследования, показывающие, что введение препаратов нормальной флоры улучшает состояние кожи (Aspergillus, Bifida Ferment Lysate, Lactobacillus/Rye Flour Ferment Filtrate). Они показывают, что одним из перспективных направлений в лечении акне [28] (и не только) могут стать про- и пребиотики, препараты на их основе.
Из-за сложных систем взаимодействия микро- и макроорганизмов результат не всегда предсказуем. Изучение функции микробиома в норме и патологии — актуальная задача медицины. И еще предстоит ответить на много вопросов.
Благодарим за прочтение статьи! С удовольствием ответим на ваши вопросы в комментариях.