Структура кожи
Кожа состоит из 3 слоев: эпидермиса, дермы и подкожной жировой клетчатки (ПЖК) (рис. 1). Эпидермис – самый тонкий из них, представляет собой многослойный ороговевающий эпителий. Дерма – средний слой кожи. Главным образом состоит из фибрилл структурного белка коллагена. ПЖК содержит жировые клетки – адипоциты. Толщина этих слоев может значительно варьировать в зависимости от анатомического места расположения.
Рис.1. Структура кожи
Варианты локализации
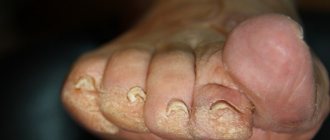
Плоскоклеточный рак кожи чаще всего представлен одиночным очагом, гораздо реже — множественными. В подавляющем большинстве случаев поражается кожа лица (нос, ушные раковины, периорбитальная область). Излюбленная локализация — переходы между слизистой оболочкой и плоским эпителием, которые наблюдаются на красной кайме губ, в перианальной области, на наружных половых органах.
В полости рта данный вид рака часто располагается на слизистой оболочке неба и языка. Для такой опухоли свойственно длительное бессимптомное течение. Она постепенно превращается в твердый узел или со временем приобретает картину перитонзиллярного абсцесса.
Плоскоклеточный рак на нижней губе возникает на фоне таких предраковых образований, как лейкоплакия, актинический и абразивный хейлит. Вначале он проявляется плотно сидящими чешуйками, под которыми образуется небольшое растущее уплотнение. Реже заболевание начинается с эрозии, которая имеет плотное основание. По мере увеличения новообразования, губа может деформироваться или уплотняться.
Для локализации рака в области вульвы, характерна локализация на переходной складке больших и малых губ, клитора. Болезнь имеет неблагоприятный прогноз, отличается быстрым метастазированием. Образованию плоскоклеточного рака кожи данной локализации может предшествовать склероатрофический лихен, болезнь Бовена, эритроплакия.
Рак кожи полового члена, как правило, возникает у мужчин старше 40 лет. Типичной локализацией для него служит задняя поверхность тела полового члена, область препуциального мешка и коронарной борозды. Предрасполагающими факторами к образованию данной опухоли служат хронические воспалительные процессы, баланит с врожденным фимозом, скопление смегмы. Именно поэтому рак полового члена практически никогда не возникает у мужчин, которые подверглись циркумцизии.
Эпидермис
Рис. 2. Эпидермис
Эпидермис – постоянно слущивающийся эпителиальный слой кожи, в котором представлены в основном из 2 типа клеток – кератиноциты и дендритные клетки. В небольшом количестве в эпидермисе присутствуют меланоциты, клетки Лангерганса, клетки Меркеля, внутриэпидермальные Т-лимфоциты. Структурно эпидермис разделяется на 5 слоев: базальный, шиповатый, зернистый, блестящий и роговой, различающиеся положением и степенью дифференцировки кератиноцитов, основной клеточной популяции эпидермиса (рис. 2).
Кератинизация. По мере дифференцировки кератиноцитов и продвижения от базального слоя до рогового происходит их кератинизация (ороговевание) – процесс, начинающийся с фазы синтеза кератина кератиноцитами и заканчивающийся их клеточной деградацией. Кератин служит строительным блоком для промежуточных филаментов. Пучки из этих филаментов, достигая цитоплазматический мембраны, формируют десмосомы, необходимые для образования прочных контактов между соседними клетками. Далее, по мере процесса эпителиальной дифференцировки, клетки эпидермиса вступают в фазу деградации. Ядра и цитоплазматические органеллы разрушаются и исчезают, обмен веществ прекращается, и наступаетапоптозклетки, когда она полностью кератинизируется (превращается в роговую чешуйку).
Базальный слой эпидермиса состоит из одного ряда митотически активных кератиноцитов, которые делятся в среднем каждые 24 часа и дают начало новым клеткам новым клеткам вышележащих эпидермальных слоев. Они активируются только в особых случаях, например при возникновении раны. Далее новая клетка, кератиноцит, выталкивается в шиповатый слой, в котором она проводит до 2 недель, постепенно приближаясь к гранулярному слою. Движение клетки до рогового слоя занимает еще 14 дней. Таким образом, время жизни кератиноцита составляет около 28 дней.
Надо заметить, что не все клетки базального слоя делятся с такой скоростью, как кератиноциты. Эпидермальные стволовые клетки в нормальных условиях образуют долгоживущую популяцию с медленным циклом пролиферации.
Шиповатый слой эпидермиса состоит из 5-10 слоев кератиноцитов, различающихся формой, структурой и внутриклеточным содержимым, что определяется положением клетки. Так, ближе к базальному слою, клетки имеют полиэдрическую форму и круглое ядро, но по мере приближения клеток к гранулярному слою они становятся крупнее, приобретают более плоскую форму, в них появляются ламеллярные гранулы, в избытке содержащие различные гидролитические ферменты. Клетки интенсивно синтезируют кератиновые нити, которые, собираясь в промежуточные филаменты, остаются не связанными со стороны ядра, но участвуют в образовании множественных десмосом со стороны мембраны, формируя связи с соседними клетками. Присутствие большого количества десмосом придает этому слою колючий вид, за что он и получил название «шиповатый».
Зернистый слой эпидермиса составляют еще живые кератиноциты, отличающиеся своей уплощенной формой и большим количеством кератогиалиновых гранул. Последние отвечают за синтез и модификацию белков, участвующих в кератинизации. Гранулярный слой является самым кератогенным слоем эпидермиса. Кроме кератогиалиновых гранул кератиноциты этого слоя содержат в большом количестве лизосомальные гранулы. Их ферменты расщепляют клеточные органеллы в процессе перехода кератиноцита в фазу терминальной дифференцировки и последующего апоптоза. Толщина гранулярного слоя может варьировать, ее величина, пропорциональная толщине вышележащего рогового слоя, максимальна в коже ладоней и подошв стоп.
Блестящий слой эпидермиса (назван так за особый блеск при просмотре препаратов кожи на световом микроскопе) тонкий, состоит из плоских кератиноцитов, в которых полностью разрушены ядра и органеллы. Клетки наполнены элейдином – промежуточной формой кератина. Хорошо развит лишь на некоторых участках тела – на ладонях и подошвах.
Роговой слой эпидермиса представлен корнеоцитами (мертвыми, терминально-дифференцированными кератиноцитами) с высоким содержанием белка. Клетки окружены водонепроницаемым липидным матриксом, компоненты которого содержат соединения, необходимые для отшелушивания рогового слоя (рис. 3). Физические и биохимические свойства клеток в роговом слое различаются в зависимости от положения клетки внутри слоя, направляя процесс отшелушивания наружу. Например, клетки в средних слоях рогового слоя обладают более сильными водосвязывающими свойствами за счет высокой концентрации свободных аминокислот в их цитоплазме.
Рис. 3. Схематичное изображение рогового слоя с нижележащим зернистым слоем эпидермиса.
Регуляция пролиферации и дифференцировки кератиноцитов эпидермиса. Являясь непрерывно обновляющейся тканью, эпидермис содержит относительно постоянное число клеток и регулирует все взаимодействия и контакты между ними: адгезию между кератиноцитами, взаимодействие между кератиноцитами и мигрирующими клетками, адгезию с базальной мембраной и подлежащей дермой, процесс терминальной дифференцировки в корнеоциты. Основной механизм регуляции гомеостаза в эпидермисе поддерживается рядом сигнальных молекул – гормонами, факторами роста и цитокинами. Кроме этого, эпидермальный морфогенез и дифференцировка частично регулируются подлежащей дермой, которая играет критическую роль в поддержании постнатальной структуры и функции кожи.
Лечение гиперкератоза
При возникновении симптомов гиперкератоза следует обращаться к дерматологу. Для опытного, квалифицированного специалиста не представляет сложностей диагностировать наличие гиперкератоза. Только лишь в единичных случаях для уточнения природы образований требуется провести биопсию подозрительных участков кожи.
Для эффективного устранения проблемы гиперкератоза, особенно поразившего кожу лица, требуется комплексная терапия. Обязательно также назначают лечение заболевания, спровоцировавшего его развитие, если таковое было обнаружено. Для этого больному может потребоваться консультация не только дерматолога, но и эндокринолога или другого узкого специалиста.
В рамках лечения непосредственно гиперкератоза назначают медикаментозную терапию и проведение косметологических процедур. Первая заключается в использовании ретиноидов, витамина С, иногда топических кортикостероидов. Для более быстрого восстановления кожи и устранения косметических недостатков показано проведение:
- парафинотерапии;
- мягких химических пилингов;
- УФ-терапии;
- мезотерапии.
Использование скрабов и других средств для механического отшелушивания не показано при гиперкератозе. Подобное лишь усугубит ситуацию и может привести к инфицированию кожи. Но всегда рекомендуется наносить на кожу эмоленты, которые увлажняют и смягчают кожу. Они содержат естественные липиды или натуральные масла, которые питают сухую кожу и насыщают необходимыми ей веществами. В результате удается восстановить естественную защиту кожи и вернуть ей природную гладкость.
При себорейном гиперкератозе, сопровождающемся образованием наростов, может быть проведено их удаление с помощью электрокоагуляции, лазера или методом криодеструкции.
К сожалению, нередко гиперкератозы сопровождают хронические заболевания, полностью устранить которые невозможно. Добиться выздоровления можно только в тех ситуациях, когда утолщение, шелушение кожи обусловлено действием механических факторов или заболеваниями, поддающимися лечению, например микозом. В остальных случаях, когда сухость и утолщение кожи вызваны хроническими дерматологическими или другими патологиями, возможно лишь снизить частоту их обострений и тяжесть течения, т. е. добиться стойкой и продолжительной ремиссии. Но это требует правильного подбора тактики лечения, постоянного ухода за кожей, а нередко и соблюдения диеты.
Медикаментозная терапия
В первую очередь назначается внутрь и наружно витамин А, называемый еще ретинолом, витамин С. В норме человек получает необходимые витамины с продуктами питания, но сегодня редко кто может похвастаться сбалансированным рационом.
Витамин А, кроме регулирования клеточного роста, необходим для поддержания остроты зрения, роста волос и ногтей, а также выполняет ряд других функций. При гиперкератозе витамин А в виде синтетических производных, называемых ретиноидами, используется для общей и местной терапии.
Одними из ярких представителей препаратов этого рода являются Роаккутан, в котором в качестве действующего вещества выступает изотретиноин, и Неотигазон, содержащий ацитретин. Это соединения являются производными ретиноевой кислоты. В случае же развития фолликулярного гиперкератоза показано использование топических ретиноидов, в частности адапалена.
Если гиперкератоз, в особенности фолликулярный, сопровождается воспалительным процессом, назначаются топические кортикостероиды, например, средства на основе гидрокортизона, преднизолона, флуацинолона, клобетазола. Большинство современных препаратов этой группы выпускается в нескольких лекарственных формах: эмульсии, крема, мази. При этом от правильности ее выбора во многом зависит эффективность лечения. Дополнительно кортикостероиды способствуют ускорению отшелушивания отмерших клеток.
Парафинотерапия
Парафинотерапия представляет собой косметологическую процедуру, при которой на предварительно очищенное лицо или другие пораженные гиперкератозом участки тела кисточкой наносится специальный косметический расплавленный парафин. Процедура занимает в среднем 20—60 минут и способствует:
- мягкому удалению ороговевших клеток;
- очищению пор от загрязнений;
- активизации микроциркуляции;
- увлажнению кожи;
- уменьшению воспаления.
Пилинги
При гиперкератозе показано проведение химических пилингов, в частности с использованием таких кислот, как:
- салициловая;
- гликолевая;
- молочная;
- лимонная;
- яблочная;
- виннокаменная.
Все они оказывают хороший отшелушивающий эффект, а также дополнительно открывают поры и увлажняют кожу. В результате удается эффективно решить проблему чрезмерной сухости и шелушения кожи, а также улучшить ее тон и текстуру, восстановив бархатистость.
УФ-терапия
Ультрафиолетовое облучение способствует устранению проявлений гиперкератоза за счет подавления патогенных микроорганизмов, включая грибы, активизации кровообращения и обмена веществ, подавления воспалительного процесса, оказания регенеративного и десенсибилизирующего эффекта.
Мезотерапия
Мезотерапия – известная косметологическая процедура, которая заключается во введении внутрь кожи необходимых ей для правильного функционирования веществ с помощью многочисленных инъекций или аппаратным способом. В результате удается не только насытить ткани витаминами, но и добиться эффективного увлажнения, что способствует уменьшению проявлений гиперкератоза и улучшению состояния кожи в целом.
Таким образом, гиперкератоз является весьма распространенным нарушением, хотя лицо он затрагивает не так часто, как, например, стопы, локти, кожу голеней и спину. Тем не менее при чрезмерной сухости и утолщении кожи лица даже в виде небольших папул возникает серьезный эстетический недостаток. Но при своевременном обращении к дерматологу и начале комплексной терапии, в том числе с использованием современных косметологических процедур, удается существенно улучшить состояние кожи лица и других участков тела или даже полностью устранить признаки гиперкератоза.
5 4 голоса
Рейтинг статьи
Дерма
Дерма представляет собой сложноорганизованную рыхлую соединительную ткань, состоящую из отдельных волокон, клеток, сети сосудов и нервных окончаний, а также эпидермальных выростов, окружающих волосяные фолликулы и сальные железы. Клеточные элементы дермы представлены фибробластами, макрофагами и тучными клетками. Лимфоциты, лейкоциты и другие клетки способны мигрировать в дерму в ответ на различные стимулы.
Дерма, составляя основной объем кожи, выполняет преимущественно трофическую и опорную функции, обеспечивая коже такие механические свойства, как пластичность, эластичность и прочность, необходимые ей для защиты внутренних органов тела от механических повреждений. Также дерма удерживает воду, участвует в терморегуляции и содержит механорецепторы. И, наконец, ее взаимодействие с эпидермисом поддерживает нормальное функционирование этих слоев кожи.
В дерме нет такого направленного и структурированного процесса клеточной дифференцировки, как в эпидермисе, тем не менее в ней также прослеживается четкая структурная организация элементов в зависимости от глубины их залегания. И клетки, и внеклеточный матрикс дермы также подвергаются постоянному обновлению и ремоделированию.
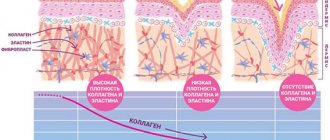
Внеклеточный матрикс (ВКМ) дермы, или межклеточное вещество, в состав которого входят различные белки (главным образом коллаген, эластин), гликозаминогликаны, самым известным из которых является гиалуроновая кислота, и протеогликаны (фибронектин, ламинин, декорин, версикан, фибриллин). Все эти вещества секретируются фибробластами дермы. ВКМ представляет собой не беспорядочное скопление всех компонентов, а сложноорганизованную сеть, состав и архитектоника которой определяют такие биомеханические свойства кожи, как жесткость, растяжимость и упругость. К белкам ВКМ прикрепляются кератиноциты эпидермиса, которые тесно состыкованы друг с другом. Именно они и формируют плотный защитный слой кожи. Структура ВКМ также способна оказывать регулирующее влияние на погруженные в него клетки. Регуляция может быть как прямой, так и косвенной. В первом случае белки и гликозаминогликаны ВКМ непосредственно взаимодействуют с рецепторами клеток и инициируют в них специфические пути передачи сигнала. Косвенная регуляция осуществляется посредством действия цитокинов и ростовых факторов, удерживаемых в ячейках сети ВКМ и высвобождаемых в определенный момент для взаимодействия с рецепторами клеток. Структурная сеть ВКМ подвергается ремоделированию ферментами из семейства матриксных металлопротеиназ (ММР). В частности, ММР-1 и ММР-13 инициируют деградацию коллагенов I и III типов. Плотность сети ВКМ дермы неравномерна – в папиллярном слое она более рыхлая, в ретикулярном — значительно плотнее как за счет более близкого расположения волокон структурных белков, так и за счет увеличения диаметра этих волокон.
Коллаген – один из главных компонентов ВКМ дермы. Синтезируется фибробластами. Процесс его биосинтеза сложный и многоступенчатый, в результате которого фибробласт секретирует в экстрацеллюлярное пространство проколлаген, состоящий из трех полипептидных α-цепей, свернутых в одну тройную спираль. Затем мономеры проколлагена ферментивным путем собираются в протяженные фибриллярные структуры различного типа. Всего в коже не менее 15 типов коллагена, в дерме больше всего I, III и V типов этого белка: 88, 10 и 2% соответственно. Коллаген IV типа локализуется в зоне базальной мембраны, а коллаген VII типа, секретируемый кератиноцитами, играет роль адаптерного белка для закрепления фибрилл ВКМ на базальной мембране (рис. 4). Волокна структурных коллагенов I, III и V типов служат каркасом, к которому присоединяются другие белки ВКМ, в частности коллагены XII и XIV типов. Считается, что эти минорные коллагены, а также небольшие протеогликаны (декорин, фибромодулин и люмикан) регулируют формирование структурных коллагеновых волокон, их диаметр и плотность образуемой сети. Взаимодействие олигомерных и полимерных комплексов коллагена с другими белками, полисахаридами ВКМ, разнообразными факторами роста и цитокинами приводит к образованию особой сети, обладающей определенной биологической активностью, стабильностью и биофизическими характеристиками, важными для нормального функционирования кожи. В папиллярном слое дермы волокна коллагена располагаются рыхло и более свободно, тогда как ее ретикулярный слой содержит более крупные тяжи коллагеновых волокон.
Рис. 4. Схематичное представление слоев кожи и распределения коллагенов разных типов.
Коллаген постоянно обновляется, деградируя под действием протеолитических ферментов коллагеназ и замещаясь вновь синтезированными волокнами. Этот белок составляет 70% сухого веса кожи. Именно коллагеновые волокна «держат удар» при механическом воздействии на нее.
Эластин формирует еще одну сеть волокон в дерме, наделяя кожу такими качествами, как упругость и эластичность. По сравнению с коллагеном эластиновые волокна менее жесткие, они скручиваются вокруг коллагеновых волокон. Именно с эластиновыми волокнами связываются такие белки, как фибулины и фибриллины, с которыми, в свою очередь, связывается латентный TGF-β-связывающий белок (LTBP). Диссоциация этого комплекса приводит к высвобождению и к активации TGF-β, самого мощного из всех факторов роста. Он контролирует экспрессию, отложение и распределение коллагенов и других матриксных белков кожи. Таким образом, интактная сеть из волокон эластина служит депо для TGF-β.
Гиалуроновая кислота (ГК) представляет собой линейный полисахарид, состоящий из повторяющихся димеров D-глюкуроновой кислоты и N-ацетилглюкозамина. Количество димеров в полимере варьирует, что приводит к образованию молекул ГК разного молекулярного веса и длины — 1х105-107 Да (2-25 мкм), оказывающих, соответственно, различный биологический эффект.
ГК — высокогидрофильное вещество, влияющее на движение и распределение воды в матриксе дермы. Благодаря этому ее свойству наша кожа в норме и в молодости обладает высоким тургором и сопротивляемостью механическому давлению.
ГК с легкостью образует вторичные водородные связи и внутри одной молекулы, и между соседними молекулами. В первом случае они обеспечивают формирование относительно жестких спиральных структур. Во втором – происходит ассоциация с другими молекулами ГК и неспецифическое взаимодействие с клеточными мембранами, что приводит к образованию сети из полимеров полисахаридов с включенными в нее фибробластами. На длинную молекулу ГК, как на нить, «усаживаются» более короткие молекулы протеогликанов (версикана, люмикана, декорина и др.), формируя агрегаты огромных размеров. Протяженные во всех направлениях, они создают каркас, внося вклад в стабилизацию белковой сети ВКМ и фиксируя фибробласты в определенном окружении матрикса. В совокупности все эти свойства ГК наделяют матрикс определенными химическими характеристиками – вязкостью, плотностью «ячеек» и стабильностью. Однако сеть ВКМ является динамической структурой, зависящей от состояния организма. Например, в условиях воспаления агрегаты ГК с протеогликанами диссоциируют, а образование новых агрегатов между вновь синтезированными молекулами ГК (обновляющимися каждые 3 дня) и протеогликанами блокируется. Это приводит к изменению пространственной структуры матрикса: увеличивается размер его ячеек, меняется распределение всех волокон, структура становится более рыхлой, клетки меняют свою форму и функциональную активность. Все это сказывается на состоянии кожи, приводя к снижению ее тонуса.
Помимо регуляции водного баланса и стабилизации ВКМ, ГК выполняет важную регуляторную роль в поддержании эпидермального и дермального гомеостаза. ГК активно регулирует динамические процессы в эпидермисе, включая пролиферацию и дифференцировку кератиноцитов, окислительный стресс и воспалительный ответ, поддержание эпидермального барьера и заживление раны. В дерме ГК также регулирует активность фибробластов и синтез коллагена. Ремоделируя матрикс, ГК управляет функционированием клеток в матриксе, влияя на их доступность для различных факторов роста и изменяя их функциональную активности. От действия ГК зависит миграция клеток и иммунный ответ в ткани. Таким образом, изменения в распределении, организации, молекулярном весе и метаболизме ГК имеют значимые физиологические последствия.
Фибробласты представляют собой основной тип клеточных элементов дермы. Именно эти клетки отвечают за продукцию ГК, коллагена, эластина, фибронектина и многих других белков межклеточного матрикса, необходимых для формирования соединительной ткани. Фибробласты в различных слоях дермы различаются и морфологически, и функционально. От глубины их залегания в дерме зависит не только количество синтезируемого ими коллагена, но и соотношение типов этого коллагена, например I и III типов, а также синтез коллагеназы: фибробласты более глубоких слоев дермы производят меньшее ее количество. Вообще, фибробласты – очень пластичные клетки, способные менять свои функции и физиологический ответ и даже дифференцироваться в другой тип клеток в зависимости от полученного стимула. В роли последнего могут выступать и сигнальные молекулы, синтезированные соседними клетками, и перестройка окружающего ВКМ.
Причины возникновения и факторы риска
В настоящее время выявлено несколько факторов, которые могут предрасполагать к возникновению плоскоклеточного рака. К ним относятся:
- Возраст. У молодых людей заболевание почти не встречается. Основная масса пациентов — пожилые люди старше 65 лет.
- Светлый цвет кожи и наличие веснушек.
- Повышенная инсоляция. Вывод о влиянии данного фактора был сделан в связи с тем, что эта форма злокачественной опухоли всегда появляется на открытых участках тела, которые постоянно подвергаются воздействию солнечного света. Кроме того, плоскоклеточный рак кожи может возникать на месте серьезных солнечных ожогов.
- Мутация гена TP53, который отвечает за подавление роста опухоли.
- Наличие предраковых образований и другие патологические состояния кожи (рубцовые атрофии, лучевые повреждения, туберкулезная волчанка, профессиональные заболевания, красный плоский лишай и др.).
- Действие на кожу канцерогенов (мышьяка, парафина, керосина, каменноугольной смолы и др.), которое приводит к воспалению и атрофии. В результате происходит образование очаговых пролифератов, которые со временем могу переродиться в злокачественное образование.
- Продолжительное механическое раздражение или повреждение кожи.
- Наличие у пациента иммуносупрессии.
- Инфицирование вирусом папилломы человека. Доказана роль некоторых его типов в возникновении рака кожи полового члена, заднего прохода, вульвы.
- Имеются научные данные о развитии этой опухоли у пациентов с псориазом после получения курсов ПУВА-терапии и фотохимиотерапии, а также у больных после лучевой терапии.
Определение причины появления плоскоклеточного рака кожи является крайне важным для оценки риска рецидивирования и метастатического распространения. Так, злокачественная опухоль, которая развилась на месте поражения кожи актиническим кератозом, метастазирует лишь в 0,5% случаев. В то же время рак, возникший на рубце, имеет гораздо более высокий риск распространения — до 30%.
Запись на консультацию круглосуточно
+7+7+78
Подкожно-жировая клетчатка
Подкожно-жировая клетчатка, или гиподерма, — самый нижний слой кожи, располагается под дермой. Состоит из жировых долек, разделенных между собой соединительнотканными септами, содержащими коллаген и пронизанными крупными сосудами. Главными клетками жировых долек являются адипоциты, количество которых варьирует в различных областях тела. В настоящее время ПЖК рассматривают не только как энергетическое депо, но и как эндокринный орган, адипоциты которого участвуют в выработке ряда гормонов (лептина, адипонектина, резистина), цитокинов и медиаторов, оказывающих влияние на метаболизм, чувствительность к инсулину, функциональную активность репродуктивной и иммунной систем.
Классификация
Существует несколько принципов классификации плоскоклеточного рака кожи. По гистологическому строению выделяется 4 типа данного новообразования, а согласно стадированию TNM — 4 стадии, каждая из которых отражает распространенность процесса в организме.
Согласно гистологической классификации выделяют следующие варианты:
- Веретеноклеточный тип, для которого характерен неблагоприятный прогноз из-за его быстрого инвазивного роста, а также склонности к метастазированию и рецидивированию.
- Акантолитический тип. Появляется на коже, пораженной актиническим кератозом.
- Веррукозный плоскоклеточный рак кожи сопровождается явлениями выраженного гиперкератоза, что клинически проявляется образованием рогового нароста (кожного рога).
- Лимфоэпителиальный тип состоит из низкодифференцированных клеток. Есть мнение, что это новообразование является опухолью придатков кожи, а не истинным плоскоклеточным раком.
Стадию развития данного типа рака определяют по размеру первичной опухоли, степени прорастания в подлежащие ткани и наличию отдаленных метастазов. Первой стадии соответствует образование размером менее 2 см, второй и третьей — более крупные опухоли с распространением в ближайшие ткани, а четвертой — очаг любых размеров с наличием метастатических поражений.
Прогноз
При выявлении плоскоклеточного рака кожи размером менее 2 см и проведении адекватного лечения, показатель 5-летней выживаемости достигает 90%. Если опухоль имеет больший размер, и наблюдается прорастание в ткани, то данный показатель снижается до 50%.
Особенно неблагоприятным прогнозом обладают опухоли, которые расположены на коже периорбитальной области, наружного слухового прохода, носогубной складки. При такой локализации новообразование может прорасти в мышцы и кости, может вызывать кровотечение из-за поражения сосудов, осложняющееся инфекциями.
Способы диагностики
Поскольку давно доказана прямая зависимость эффективности проведенного лечения от стадии злокачественного новообразования, на которой оно было обнаружено, выделяют два уровня диагностики плоскоклеточного рака кожи: раннюю и позднюю.
Ранним считается постановка диагноза на I-II стадии. В этом случае возможно полное выздоровление больного при условии выбора правильной тактики лечения. Позднее выявление — это постановка диагноза на III и IV стадии. Прогноз, как правило, неблагоприятен по причине сложности проведения или невозможности оперативного лечения.
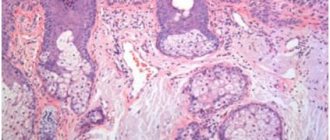
«Золотой стандарт» диагностики плоскоклеточного рака кожи — биопсия с последующим гистологическим исследованием. Особенно информативным считается иммуногистохимический метод. Так как опухоль является наружной и получить биоматериал для проведения гистологии несложно, новообразование верифицируется в 99% случаев.
Также широко применяется метод дерматоскопии. В этом случае в пользу рака кожи говорит наличие центральных кератиновых пробок, расширенных и разветвленных сосудов на поверхности.
При любой форме плоскоклеточного рака, наряду с тщательным сбором анамнеза и физикальным осмотром, специалист должен провести оценку состояния лимфоузлов. При подозрении на наличие метастатических очагов, основным диагностическим методом служит тонкоигольная аспирация. Также возможно назначение дополнительных методов визуализации (УЗИ, рентгенография, КТ, ангиография) для выявления регионарных и отдаленных метастазов.
Профилактика
Главной мерой профилактики плоскоклеточного рака кожи является своевременное выявление и лечение предраковых состояний. В связи с этим, молодым людям рекомендовано проходить осмотр у дерматолога каждые 3 года, а людям старше 40 лет — каждый год. При обнаружении любых изменений на коже, также следует обращаться к специалисту.
Очаги хронического воспаления на коже должны подвергаться адекватной санации. Также следует избегать многократного повреждения одного и того же кожного участка (натирания, сдавления тесной одеждой и обувью, травмирования во время однообразной ручной работы).
Немаловажным является соблюдение солнечного режима и использование крема с солнцезащитным компонентом, отказ от посещения солярия. При работе с химическими реагентами — источниками профессиональной вредности, необходимо применять индивидуальные средства защиты кожи.
Запись на консультацию круглосуточно
+7+7+78